Οι εικονιζόμενοι δεν είναι πραγματικοί ασθενείς.
ΕΝΔΕΙΞΗ
Το Dupixent ενδείκνυται σε ενήλικες ως πρόσθετη θεραπεία συντήρησης για τη μη ελεγχόμενη χρόνια αποφρακτική πνευμονοπάθεια (ΧΑΠ) που χαρακτηρίζεται από αυξημένο αριθμό ηωσινοφίλων στο αίμα σε συνδυασμό με ένα εισπνεόμενο κορτικοστεροειδές (ICS), έναν β2-αγωνιστή μακράς δράσης (LABA) και έναν μουσκαρινικό ανταγωνιστή μακράς δράσης (LAMA), ή σε συνδυασμό με έναν LABA και έναν LAMA εάν το ICS δεν ενδείκνυται.
Μηχανισμός της νόσου/ Μηχανισμός Δράσης
Το DUPIXENT είναι ο πρώτος και μοναδικός βιολογικός παράγοντας που στοχεύει τη φλεγμονή τύπου 2 στη ΧΑΠ1
Παρακολουθήστε για να μάθετε πώς δρα το DUPIXENT
Οι IL-4 και IL-13 αποτελούν βασικές και κεντρικές κυτταροκίνες της φλεγμονής τύπου 22
|
|
|
Η IL-4 συντηρεί τη φλεγμονή τύπου 2, προάγοντας τη διαφοροποίηση των Th0 σε Th2.3 |
Η IL-13 προάγει την υπερπλασία των κυψελιδικών κυττάρων |
|
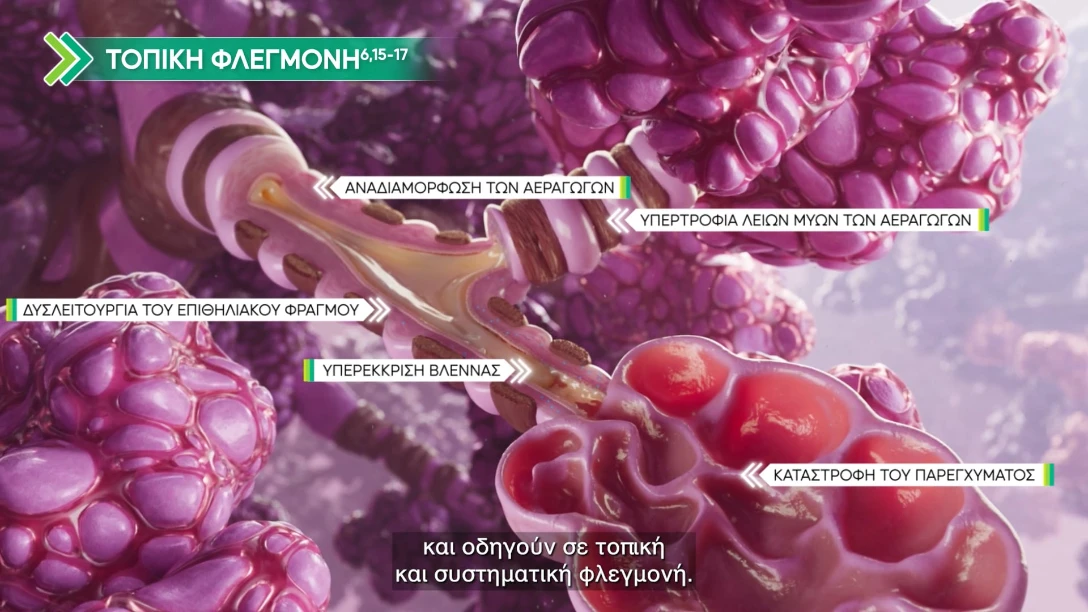
Τοπική φλεγμονή3-6 |
Συστηματική φλεγμονή3 |
|
|
-
Δύσπνοια
-
Βήχας
-
Παραγωγή πτυέλων
-
Το DUPIXENT, μέσω της διπλής αναστολής των IL-4 και IL-13, όταν χορηγήθηκε σε συνδυασμό
με βέλτιστη εισπνεόμενη θεραπεία,a κατέδειξε βελτίωση των συμπτωμάτων.1,8
aΤριπλή εισπνεόμενη θεραπεία ή διπλή εισπνεόμενη θεραπεία εάν τα ICS αντενδείκνυνται.1
Αναγνωριστικό Ασθενούς

Ο ασθενής σας μπορεί να είναι κατάλληλος υποψήφιος για το DUPIXENT1,7-9

Φλεγμονή τύπου 2: Αυξημένα επίπεδα ηωσινοφίλων στο αίμα (≥300 κύτταρα/μL)

Παραμένει συμπτωματικός παρά τη βέλτιστη εισπνεόμενη θεραπείαa: Δύσπνοια, βήχας και βλέννη
Παροξύνσεις: Υπέστη μέτριες παροξύνσεις ή τουλάχιστον 1 σοβαρή παρόξυνση κατά το προηγούμενο έτος
Το προφίλ ασθενούς είναι υποθετικό και δεν αφορά πραγματικό άτομο.
a Τριπλή εισπνεόμενη θεραπεία ή διπλή εισπνεόμενη θεραπεία εάν τα εισπνεόμενα κορτικοστεροειδή δεν ενδείκνυνται.1
Η αυξημένη συγκέντρωση ηωσινοφίλων στο αίμα αναγνωρίζεται από την Έκθεση GOLD 2025 ως κλινικά χρήσιμος βιοδείκτης για την ταυτοποίηση της ΧΑΠ με φλεγμονή τύπου 2.7
Δείτε τα ιατρικά ιστορικά του Γιάννη και της Μαρίας
Ιατρικό ιστορικό Γιάννη
Ηλικία 63
Το προφίλ ασθενούς είναι ενδεικτικό και δεν αφορά πραγματικό ασθενή.
«Είναι δύσκολο να βγάλω τη μέρα στη δουλειά. Πρέπει να κάθομαι και να ξεκουράζομαι πριν ολοκληρώσω τη διανομή της αλληλογραφίας μου. Και το να αποβάλλω τόσο πολύ φλέγμα είναι επίπονο. Θέλω να εργάζομαι μέχρι τα 70 και να απολαύσω τη συνταξιοδότηση με την οικογένειά μου, αλλά δεν είμαι σίγουρος ότι η ΧΑΠ μου θα το επιτρέψει.»
-
Σε βέλτιστη εισπνεόμενη θεραπεία (ICS, LAMA, LABA· 1 δόση ημερησίως)
-
Ενδείξεις φλεγμονής τύπου 21,7: αυξημένα επίπεδα ηωσινοφίλων στο αίμα (310 κύτταρα/μL)
-
2 μέτριες παροξύνσεις που απαιτούσαν θεραπεία με συστηματικά κορτικοστεροειδή (OCS) το τελευταίο έτος
-
Διακοπή καπνίσματος στην ηλικία των 43 ετών, ιστορικό καπνίσματος 15 πακέτα-έτη
-
4 έτη από τη διάγνωση της ΧΑΠ
-
FVC: 2,7 L; FEV1/FVC: 0,67; μετα-βρογχοδιασταλτικό FEV1: 1,8 L (65% της προβλεπόμενης τιμής)
Στόχος θεραπείας:
Βελτίωση της αναπνοής, μείωση της βλέννας, ποιοτικός χρόνος με την οικογένεια.
Πρόκληση στη θεραπεία:
Ο Γιάννης παραμένει συμπτωματικός παρά τη συνεχή λήψη βελτιστοποιημένης εισπνεόμενης θεραπείας για 14 μήνες.
Κλινικό ιστορικό της Μαρίας
Ηλικία 74 ετών
Το προφίλ του ασθενούς είναι ενδεικτικό και δεν αφορά πραγματικό ασθενή.
«Νοσηλεύτηκα στη ΜΕΘ νωρίτερα φέτος. Παλαιότερα μπορούσα να βγαίνω για δουλειές, αλλά τώρα είμαι δεμένη με το οξυγόνο στο σπίτι. Με δυσκολία φτάνω μέχρι το γραμματοκιβώτιό μου. Φοβάμαι ότι αν ξαναμπώ στο νοσοκομείο, ίσως να μην επιστρέψω ποτέ ξανά στο σπίτι μου.»
-
Σε βέλτιστη εισπνεόμενη θεραπεία (LAMA, LABA· 1 δόση την ημέρα)
-
Ένδειξη φλεγμονής τύπου 21,7: αυξημένα επίπεδα ηωσινόφιλων στο αίμα (480 κύτταρα/μL)
-
1 σοβαρή παρόξυνση που απαίτησε νοσηλεία το τελευταίο έτος
-
Διακοπή καπνίσματος στην ηλικία των 73 ετών, ιστορικό καπνίσματος 35 πακέτα-έτη
-
2 έτη από τη διάγνωση της ΧΑΠ
-
FVC: 2,5 L· FEV1/FVC: 0,52· μετα-βρογχοδιασταλτικό FEV1: 1,3 L (48% της προβλεπόμενης τιμής)
Στόχος θεραπείας:
Μείωση του κινδύνου παροξύνσεων, βελτίωση της ποιότητας ζωής,απόλαυση απλών στιγμών.
Πρόκληση στη θεραπεία:
Η Μαρία διέκοψε πρόσφατα το κάπνισμα μετά από αρκετές προσπάθειες, ωστόσο οι παροξύνσεις της ήταν σοβαρές. Με κάθε παρόξυνση να αυξάνει τον κίνδυνο για περαιτέρω επεισόδια, η κατάσταση είναι επείγουσα.10
Ανακαλύψτε τι μπορεί να προσφέρει το DUPIXENT σε ασθενείς όπως η Μαρία
ΠΕΡΙΣΣΟΤΕΡΕΣ ΣΤΙΓΜΕΣ ΠΟΥ ΜΠΟΡΩ
για ασθενείς που παραμένουν συμπτωματικοί με βέλτιστα ρυθμισμένη εισπνεόμενη θεραπείαa
ΜΙΑ ΚΑΙΝΟΤΟΜΟΣ ΘΕΡΑΠΕΙΑ ΓΙΑ ΤΗ ΧΑΠ1
Αποτελεσματικότητα Παροξύνσεις
Η DUPIXENT ΜΕΙΩΣΕ ΣΗΜΑΝΤΙΚΑ ΤΙΣ ΠΑΡΟΞΥΝΣΕΙΣ1
Οι μέτριες ή σοβαρές παροξύνσεις αποτελούν σημαντικό παράγοντα κακής έκβασης στη ΧΑΠ.8
Μείωση του ρυθμού παροξύνσεων
Ετησιοποιημένος ρυθμός μέτριων ή σοβαρών παροξύνσεων ΧΑΠ στη Εβδομάδα 52 (πρωτεύον καταληκτικό σημείο)1
![]()
Κλινική μελέτη NOTUS
Μείωση του ποσοστού μέτριων ή σοβαρών παροξύνσεων1,d
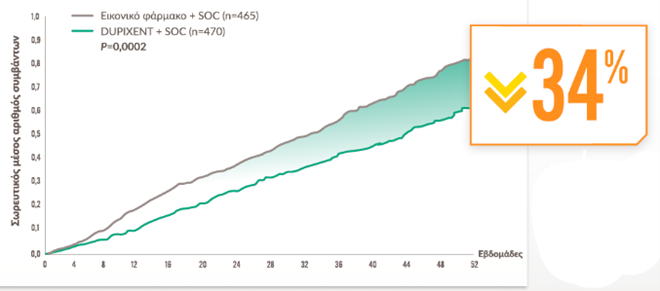
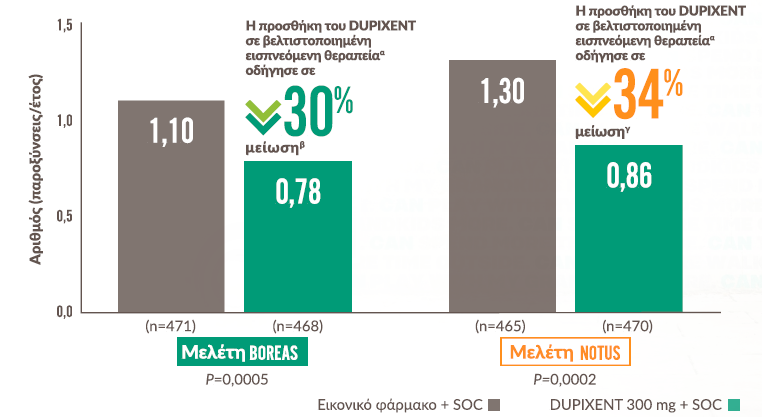
Η προσθήκη του DUPIXENT στη βέλτιστα ρυθμισμένη εισπνεόμενη θεραπείαa οδήγησε σε μείωση των μέτριων ή σοβαρών παροξύνσεων1
Ως μέτριες παροξύνσεις ορίστηκαν εκείνες που κατέληξαν σε θεραπεία με συστηματικά κορτικοστεροειδή, αντιβιοτικά ή και τα δύο.1
Ως σοβαρές παροξύνσεις ορίστηκαν εκείνες που οδήγησαν σε νοσηλεία ή παρακολούθηση για διάστημα άνω των 24 ωρών σε τμήμα επειγόντων περιστατικών ή μονάδα άμεσης φροντίδας.1
aΤριπλή εισπνεόμενη θεραπεία ή διπλή εισπνεόμενη θεραπεία εάν η χρήση ICS δεν ήταν κατάλληλη.1
bΛόγος ρυθμού έναντι εικονικού φαρμάκου: 0,71 (95% ΔΕ: 0,58, 0,86). 1
cΛόγος ρυθμού έναντι εικονικού φαρμάκου: 0,66 (95% ΔΕ: 0,54, 0,82).1
dΤο κύριο καταληκτικό σημείο ήταν ο ετήσιος ρυθμός μέτριων ή σοβαρών παροξύνσεων.1
eΤα κριτήρια ένταξης απαιτούσαν οι ασθενείς να έχουν παρουσιάσει ≥1 παρόξυνση κατά τη διάρκεια θεραπείας με SOC. 8,9

Μελέτη BOREAS
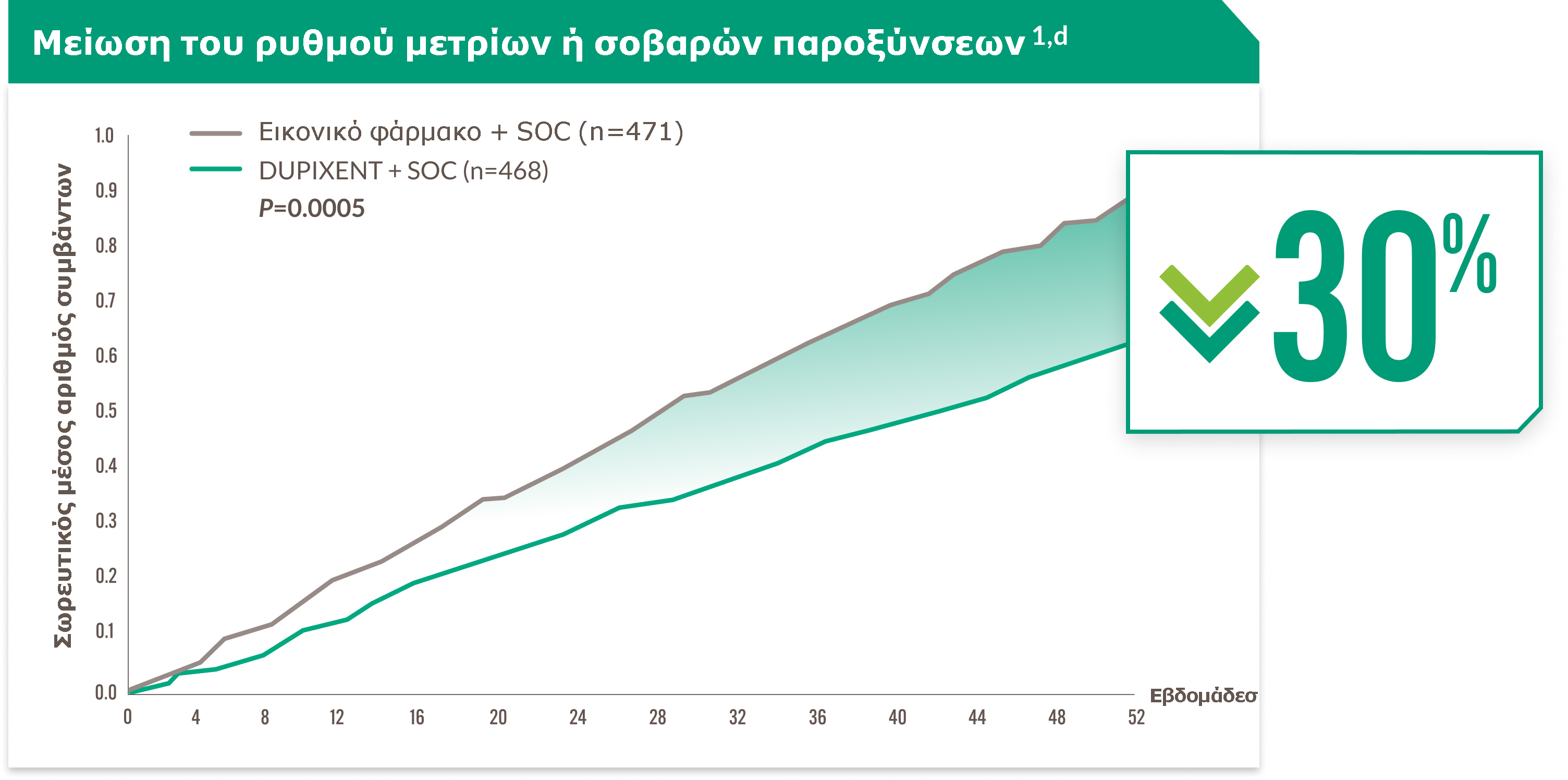
Η προσθήκη του DUPIXENT στη βέλτιστα ρυθμισμένη εισπνεόμενη θεραπείαa οδήγησε σε μείωση των μέτριων ή σοβαρών παροξύνσεων1
Ως μέτριες παροξύνσεις ορίστηκαν εκείνες που κατέληξαν σε θεραπεία με συστηματικά κορτικοστεροειδή, αντιβιοτικά ή και τα δύο.1
Ως σοβαρές παροξύνσεις ορίστηκαν εκείνες που οδήγησαν σε νοσηλεία ή παρακολούθηση για διάστημα άνω των 24 ωρών σε τμήμα επειγόντων περιστατικών ή μονάδα άμεσης φροντίδας.1
aΤριπλή εισπνεόμενη θεραπεία ή διπλή εισπνεόμενη θεραπεία εάν η χρήση ICS δεν ήταν κατάλληλη.1
bΛόγος ρυθμού έναντι εικονικού φαρμάκου: 0,71 (95% ΔΕ: 0,58, 0,86). 1
cΛόγος ρυθμού έναντι εικονικού φαρμάκου: 0,66 (95% ΔΕ: 0,54, 0,82).1
dΤο κύριο καταληκτικό σημείο ήταν ο ετήσιος ρυθμός μέτριων ή σοβαρών παροξύνσεων.1
eΤα κριτήρια ένταξης απαιτούσαν οι ασθενείς να έχουν παρουσιάσει ≥1 παρόξυνση κατά τη διάρκεια θεραπείας με SOC. 8,9
Αποτελεσματικότητα σε υποομάδες
Μείωση των παροξύνσεων παρατηρήθηκε σε βασικές υποομάδες ασθενών ανεξαρτήτως1,8,9:

|
|

|
|
Αριθμός μέτριων ή σοβαρών παροξύνσεων κατά το προηγούμενο έτος (≤2, n=371 [BOREAS] και n=381 [NOTUS]; 3, n=57 [BOREAS] και n=57 [NOTUS]; ≥4, n=40 [BOREAS] και n=32 [NOTUS])e |
Βαρύτητα νόσου κατά την έναρξη (προ βρογχοδιασταλτικό προβλεπόμενο ποσοστιαίο FEV1: <50%, n=227 [BOREAS] και n=250 [NOTUS] ή ≥50%, n=241 [BOREAS] και n=217 [NOTUS]) |
Κατάσταση καπνίσματος κατά τον έλεγχο (προηγούμενο, n=334 [BOREAS] και n=328 [NOTUS]· τρέχον, n=134 [BOREAS] και n=142 [NOTUS]) |
Ως μέτριες παροξύνσεις ορίστηκαν εκείνες που κατέληξαν σε θεραπεία με συστηματικά κορτικοστεροειδή, αντιβιοτικά ή και τα δύο.1
Ως σοβαρές παροξύνσεις ορίστηκαν εκείνες που οδήγησαν σε νοσηλεία ή παρακολούθηση για διάστημα άνω των 24 ωρών σε τμήμα επειγόντων περιστατικών ή μονάδα άμεσης φροντίδας.1
aΤριπλή εισπνεόμενη θεραπεία ή διπλή εισπνεόμενη θεραπεία εάν η χρήση ICS δεν ήταν κατάλληλη.1
bΛόγος ρυθμού έναντι εικονικού φαρμάκου: 0,71 (95% ΔΕ: 0,58, 0,86). 1
cΛόγος ρυθμού έναντι εικονικού φαρμάκου: 0,66 (95% ΔΕ: 0,54, 0,82).1
dΤο κύριο καταληκτικό σημείο ήταν ο ετήσιος ρυθμός μέτριων ή σοβαρών παροξύνσεων.1
eΤα κριτήρια ένταξης απαιτούσαν οι ασθενείς να έχουν παρουσιάσει ≥1 παρόξυνση κατά τη διάρκεια θεραπείας με SOC. 8,9
Αποτελεσματικότητα Λειτουργία των Πνευμόνων
ΠΕΡΙΣΣΟΤΕΡΕΣ ΣΤΙΓΜΕΣ ΠΟΥ ΜΠΟΡΩ με βελτιωμένη αναπνοή1
Η θεραπεία με DUPIXENT ΠΡΟΣΕΦΕΡΕ ΤΑΧΕΙΑ ΚΑΙ ΔΙΑΡΚΗ ΒΕΛΤΙΩΣΗ ΣΤΗΝ ΑΝΑΠΝΟΗ ΤΩΝ ΑΣΘΕΝΩΝ
Η λειτουργία των πνευμόνων βελτιώθηκε ήδη από την Εβδομάδα 2, με διατήρηση μέχρι την Εβδομάδα 52

Μελέτη BOREAS
Ταχεία και διατηρούμενη βελτίωση της πνευμονικής λειτουργίας1,a,b
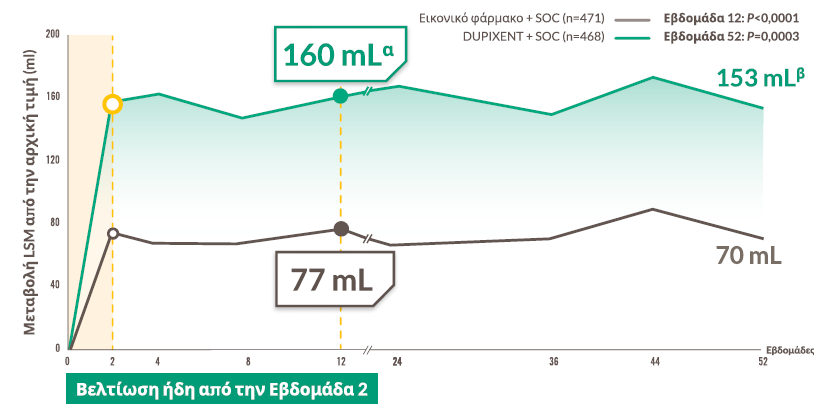
Βελτίωση ήδη από την 2η εβδομάδα
aΚύριο δευτερεύον καταληκτικό σημείο ήταν η μεταβολή LSM από την αρχική τιμή στην προ-ΒΔ FEV1 στην Εβδομάδα 12.1
bΚύριο δευτερεύον καταληκτικό σημείο ήταν η μεταβολή LSM από την αρχική τιμή στην προ-ΒΔ FEV1 στην Εβδομάδα 52.1
![]()
Κλινική μελέτη NOTUS
Ταχεία και διατηρούμενη βελτίωση της πνευμονικής λειτουργίας1,a,b
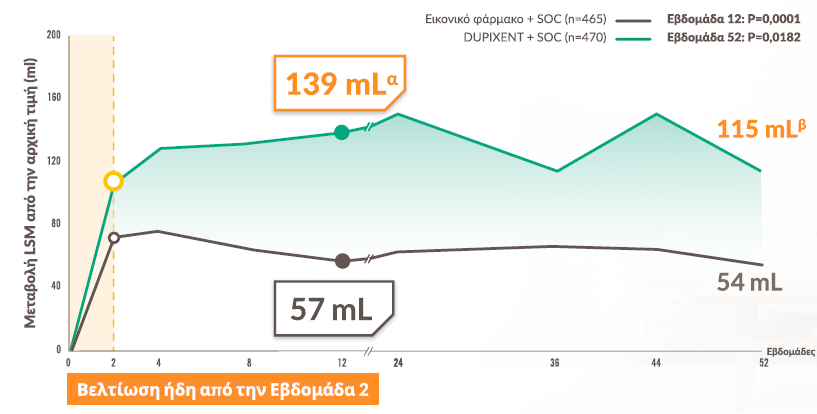
Βελτίωση ήδη από την 2η εβδομάδα
aΚύριο δευτερεύον καταληκτικό σημείο ήταν η μεταβολή LSM από την αρχική τιμή στην προ-ΒΔ FEV1 στην Εβδομάδα 12.1
bΚύριο δευτερεύον καταληκτικό σημείο ήταν η μεταβολή LSM από την αρχική τιμή στην προ-ΒΔ FEV1 στην Εβδομάδα 52.1
Ποιότητα ζωής
Βελτιωμένη ποιότητα ζωής με το DUPIXENT για ΠΕΡΙΣΣΟΤΕΡΕΣ ΣΤΙΓΜΕΣ ΠΟΥ ΜΠΟΡΩ 1
DUPIXENTaΣΗΜΑΝΤΙΚΗ ΒΕΛΤΙΩΣΗ ΤΗΣ ΠΟΙΟΤΗΤΑΣ ΖΩΗΣ ΓΙΑ ΤΟΥΣ ΠΕΡΙΣΣΟΤΕΡΟΥΣ ΑΣΘΕΝΕΙΣ ΜΕ ΧΑΠ1,8

Μελέτη BOREAS
Το 51,5% των ασθενών που έλαβαν DUPIXENTa πέτυχε κλινικά σημαντική βελτίωση στη συνολική βαθμολογία SGRQ (≥4 μονάδες) έναντι 43,1% με εικονικό φάρμακο στη 52η εβδομάδα (P=0,009)8,b,c
Στη μελέτη NOTUS, το 51,4% των ασθενών που έλαβαν DUPIXENTa πέτυχε ονομαστική βελτίωση στη συνολική βαθμολογία SGRQ έναντι 46,5% με εικονικό φάρμακο στη 52η εβδομάδα (OR: 1,16; 95% ΔΕ: 0,86, 1,58)9,b
Βελτίωση στην ποιότητα ζωής (SGRQ)1,8,b
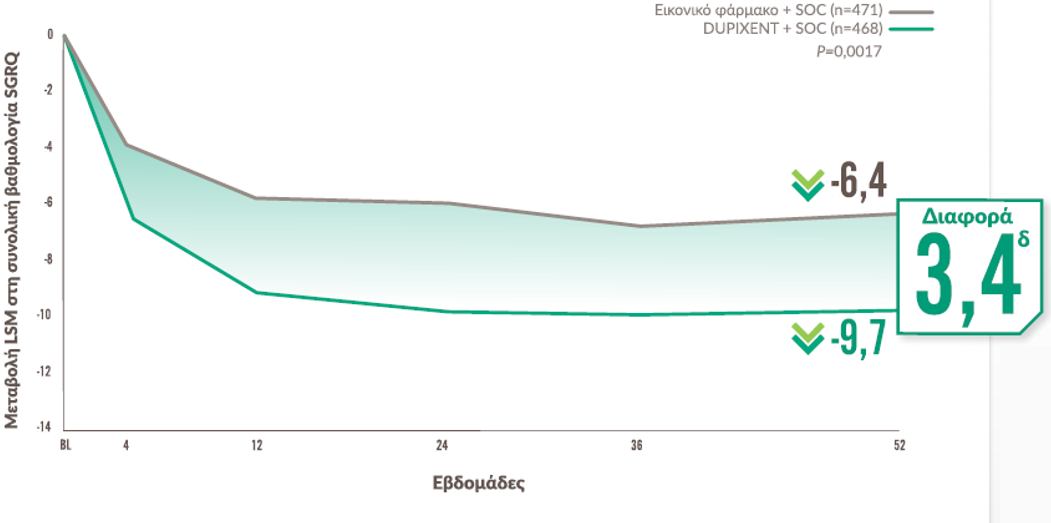
3,4 διαφοράd
Στη μελέτη NOTUS, οι ασθενείς που έλαβαν DUPIXENTa παρουσίασαν ονομαστική διαφορά LSM στη συνολική βαθμολογία SGRQ σε σύγκριση με το εικονικό φάρμακο κατά 3,37 μονάδες (95% ΔΕ: -5,81, -0,93; P=0,007).1

Βήχας |

Πτύελα |

Δύσπνοια |

Συριγμός |

Εξάρσεις |

Δραστηριότητες καθημερινής ζωής |

Φαρμακευτική αγωγή |
aΕπιπλέον της τριπλής εισπνεόμενηςθεραπείας, ήδιπλής εισπνεόμενης θεραπείας εφόσον τα ICS δεν ήταν κατάλληλα.11
bΔευτερεύον κύριο καταληκτικό σημείο ήταν το ποσοστό των ασθενών που πέτυχαν βελτίωση ≥4 μονάδων (ελάχιστα κλινικά σημαντική διαφορά) στη συνολική βαθμολογία SGRQ στη Εβδομάδα 52 (BOREAS OR: 1,4; 95% CI: 1,1, 1,9).8,9
cΤο SGRQ αποτελεί ερωτηματολόγιο 50 ερωτήσεων σχεδιασμένο για τη μέτρηση και ποσοτικοποίηση της κατάστασης υγείας σε ενήλικες ασθενείς με χρόνια περιορισμό της ροής του αέρα.8
dΔιαφορά LSM (BOREAS; Εβδομάδα 52): -3,36 (95% CI: -5,46, -1,27); P=0,0017.1
Βελτίωση Συμπτωμάτων
Βελτιώστε τα συμπτώματα για ΠΕΡΙΣΣΟΤΕΡΕΣ ΣΤΙΓΜΕΣ ΠΟΥ ΜΠΟΡΩ με το DUPIXENT8
Το DUPIXENT ΒΕΛΤΙΩΣΕ ΤΑ ΧΑΡΑΚΤΗΡΙΣΤΙΚΑ ΣΥΜΠΤΩΜΑΤΑ ΠΟΥ ΕΠΗΡΕΑΖΟΥΝ ΤΗΝ ΕΥΕΞΙΑ ΤΩΝ ΑΣΘΕΝΩΝ

Μελέτη BOREAS
Τα συμπτώματα αξιολογήθηκαν με τη χρήση του E-RS:COPD8,12,13,a-c

Όλα τα επιμέρους στοιχεία της βαθμολογίας E-RS:COPD παρουσίασαν βελτίωση
Η συνολική βαθμολογία του Εργαλείου Αξιολόγησης Αναπνευστικών Συμπτωμάτων στη ΧΑΠ (E-RS:COPD), ένα ερωτηματολόγιο 11 ερωτήσεων που συμπληρώνεται από τον ασθενή και χρησιμοποιείται για τη μέτρηση της επίδρασης μιας θεραπείας στη σοβαρότητά τους χρησιμοποιήθηκε σαν βάση την εβδομάδα 52.
Τα αναπνευστικά συμπτώματα σε ασθενείς με σταθερή ΧΑΠ αξιολογήθηκαν κατά την έναρξη και στη Εβδομάδα 52. Το E- RS:COPD χρησιμοποιεί τα 11 στοιχεία αναπνευστικών συμπτωμάτων που περιλαμβάνονται στο 14-στοιχείων EXACT. Οι βαθμολογίες κυμαίνονται από 0 έως 40, με χαμηλότερη βαθμολογία να υποδηλώνει χαμηλότερη βαρύτητα της νόσου.
Οι βαθμολογίες E-RS:COPD μειώθηκαν8,b,d
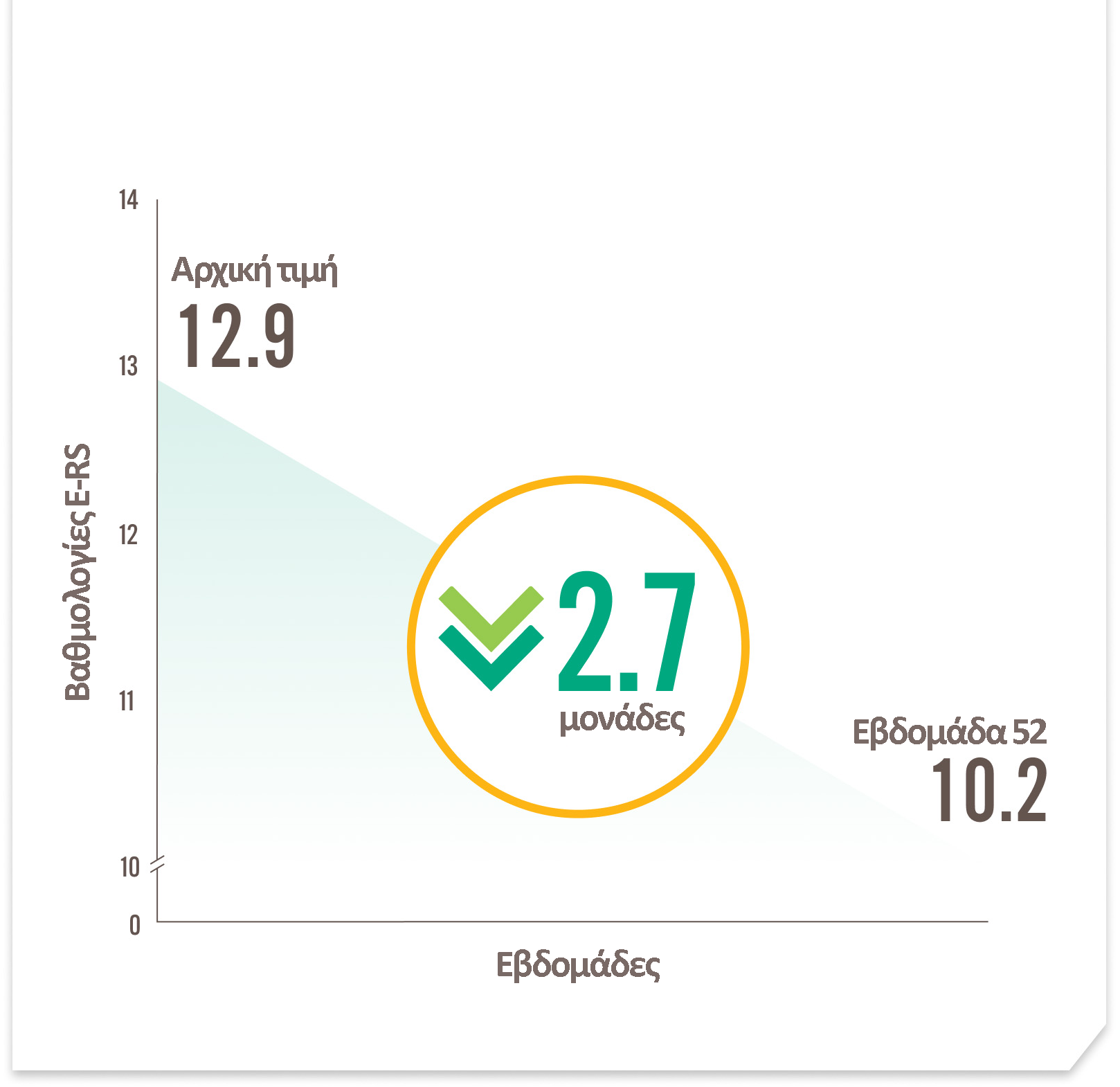
Στη μελέτη NOTUS, οι βαθμολογίες E-RS:COPD μειώθηκαν κατά 2,4 μονάδες.9
Το όριο κλινικά σημαντικής μεταβολής στη συνολική βαθμολογία E-RS:COPD είναι μείωση ≥2,0 μονάδων.14
aΕξερευνητικό καταληκτικό σημείο ήταν η μεταβολή από την έναρξη στη βαθμολογία E-RS:COPD.8
bDUPIXENT σε συνδυασμό με τριπλή εισπνεόμενη θεραπεία ή διπλή εισπνεόμενη θεραπεία εάν η χρήση ICS δεν ήταν κατάλληλη.1
cΑυτά δεν είναι τα μόνα συμπτώματα που αξιολογούνται από το E-RS:COPD.13
dΟι βαθμολογίες του E-RS:COPD κυμαίνονται από 0 έως 40, με τις υψηλότερες τιμές να υποδεικνύουν μεγαλύτερη βαρύτητα της νόσου.13
Σχεδιασμός Μελέτης
Το DUPIXENT συμπεριέλαβε ασθενείς με ΧΑΠ και φλεγμονή τύπου 2 σε 2 κλινικές μελέτες1,7
ΚΛΙΝΙΚΕΣ ΜΕΛΕΤΕΣ BOREAS ΚΑΙ NOTUS
ΑΞΙΟΛΟΓΗΘΗΚΕ Η ΑΣΦΑΛΕΙΑ, Η ΑΝΟΧΗ ΚΑΙ Η ΑΠΟΤΕΛΕΣΜΑΤΙΚΟΤΗΤΑ ΣΕ ΑΣΘΕΝΕΙΣ ΜΕ ΧΑΠ ΚΑΙ ΦΛΕΓΜΟΝΗ ΤΥΠΟΥ 21,7
Όλοι οι ασθενείς έλαβαν βέλτιστη θεραπεία SOC (ICS+LAMA+LABA ή LAMA+LABA εάν τα ICS δεν ήταν κατάλληλα)1,a
Δύο μελέτες φάσης 3, πολυκεντρικές, διεθνείς, διπλά τυφλές, τυχαιοποιημένες, με εικονικό φάρμακο ως ομάδα ελέγχου, σε ασθενείς με μη ελεγχόμενη ΧΑΠ1,8,9
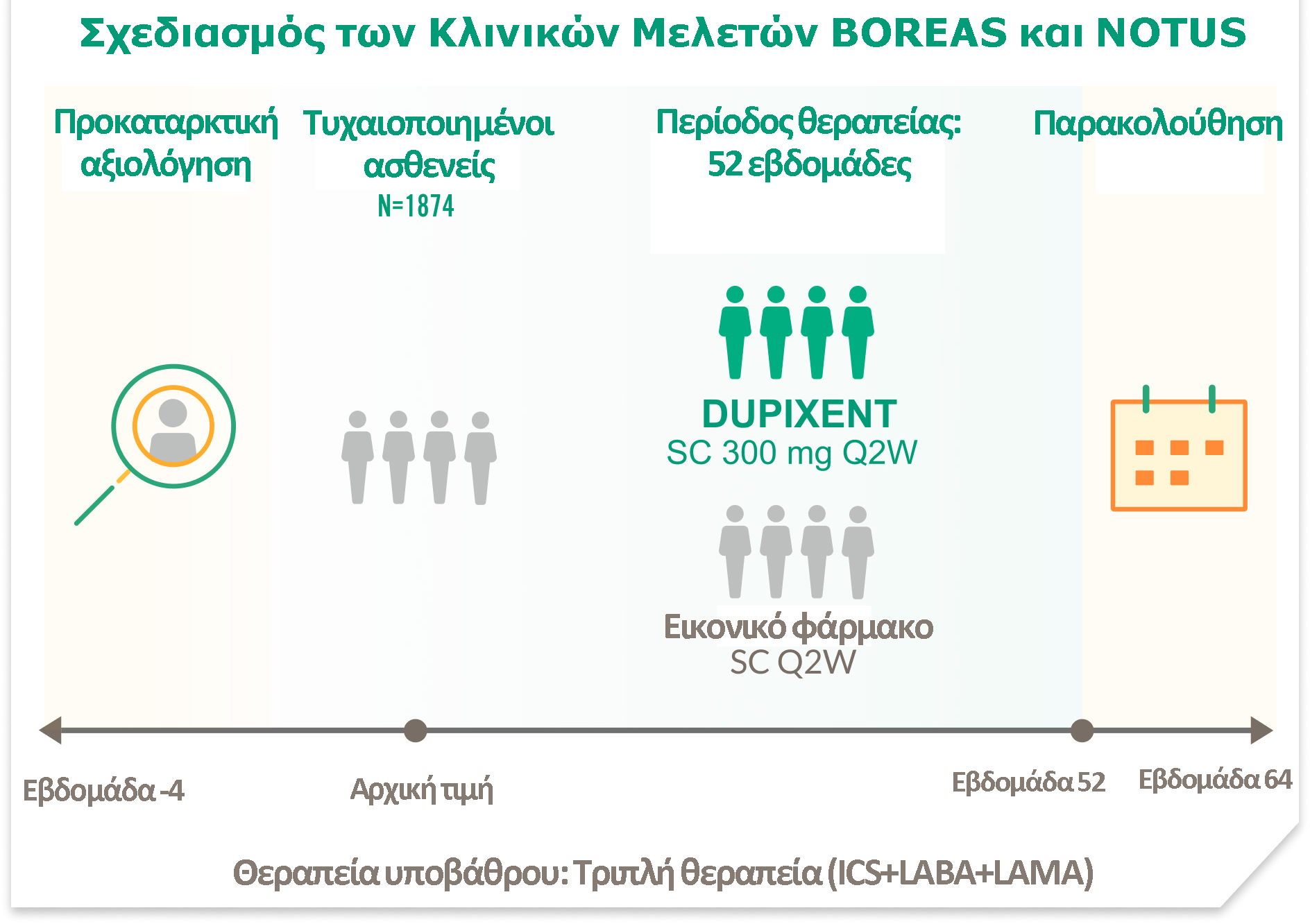
|
ΚΥΡΙΑ ΜΕΤΑΒΛΗΤΗ ΑΞΙΟΛΟΓΗΣΗΣ |
Εβδομάδα 52 |
Ετησιοποιημένος ρυθμός μέτριων ή σοβαρών παροξύνσεων της ΧΑΠ |
|
ΕΠΙΛΕΓΜΕΝΕΣ ΔΕΥΤΕΡΕΥΟΥΣΕΣ ΚΑΙ ΑΛΛΕΣ ΜΕΤΑΒΛΗΤΕΣ ΑΞΙΟΛΟΓΗΣΗΣ |
Εβδομάδα 12 Εβδομάδα 52 |
Μεταβολή στη λειτουργία των πνευμόνων (προ-BD FEV1) από την αρχική τιμή |
|
Εβδομάδα 52 |
Μεταβολή στη συνολική βαθμολογία SGRQ από την αρχική τιμή |
|
|
Εβδομάδα 52 |
Ποσοστό ασθενών με βελτίωση στη συνολική βαθμολογία SGRQ ≥4 μονάδες |
|
|
Εβδομάδα 12 Εβδομάδα 52 |
Μεταβολή στη λειτουργία των πνευμόνων (προ-BD FEV1) από την αρχική τιμή σε ασθενείς με αρχική τιμή FeNO ≥20 ppb |
|
|
Εβδομάδα 52 |
Ετησιοποιημένος ρυθμός μέτριων ή σοβαρών παροξύνσεων της ΧΑΠ σε ασθενείς με αρχική τιμή FeNO ≥20 ppb |
|
|
Εβδομάδα 52 |
Μεταβολή στη συνολική βαθμολογία E-RS:COPD από την αρχική τιμή |
a98% έλαβαν ICS+LAMA+LABA στη μελέτη BOREAS και 99% στη μελέτη NOTUS.1
|
Κύρια Κριτήρια Ένταξης8,9 |
|
Διάγνωση ΧΑΠ από ιατρό για ≥12 μήνες πριν την τυχαιοποίηση |
|
Ενεργοί ή πρώην καπνιστές με ιστορικό καπνίσματος ≥10 πακέτα-έτη |
|
Σημεία ή συμπτώματα χρόνιας βρογχίτιδας (χρόνιος παραγωγικός βήχας) για ≥3 μήνες |
|
≥1 παρόξυνση ενώ ο ασθενής λάμβανε την καθιερωμένη θεραπεία |
|
mMRC βαθμός δύσπνοιας ≥2 |
|
Αριθμός ηωσινοφίλων στο αίμα ≥300 κύτταρα/μL |
|
≥2 μέτριες ή ≥1 σοβαρή παρόξυνση εντός του έτους πριν τον προ-ελεγχο |
|
Υπόβαθρο τριπλής θεραπείας (ICS+LAMA+LABA) για 3 μήνες πριν την τυχαιοποίηση με σταθερή δόση φαρμάκου για ≥1 μήνα πριν την Επίσκεψη 1· διπλή θεραπεία (LAMA+LABA) επιτρέπεται εάν τα ICS ήταν μη κατάλληλα |
|
Κύρια Κριτήρια Αποκλεισμού8,9 |
|
Διάγνωση ΧΑΠ από ιατρό για <12 μήνες πριν την τυχαιοποίηση |
|
Διάγνωση ή ιστορικό άσθματος σύμφωνα με τις κατευθυντήριες οδηγίες GINA |
Χαρακτηριστικά ασθενών κατά την έναρξη1
|
Παράμετρος |
BOREAS (n=939) |
NOTUS (n=935) |
|---|---|---|
|
Μέση ηλικία (έτη) ± ΤΑ |
65,1 (8,1) | 65,0 (8,3) |
|
Άνδρες (%) |
66,0 | 67,6 |
|
Λευκοί (%) |
84,1 | 89,6 |
|
Pack-years (± ΤΑ) |
40,5 (23,4) | 40,3 (27,2) |
| Ενεργοί καπνιστές (%) | 30,0 | 29,5 |
|
Εμφύσημα (%) |
32,6 | 30,4 |
| Διάρκεια ΧΑΠ (έτη) ± ΤΑ | 8,8 (6,0) | 9,3 (6,4) |
| Μέτριες/σοβαρές παροξύνσεις (± ΤΑ) | 2,3 (1,0) | 2,1 (0,9) |
| Σοβαρές παροξύνσεις (± ΤΑ) | 0,3 (0,7) | 0,3 (0,6) |
| ICS/LAMA/LABA (%) | 97,6 | 98,8 |
| FEV1/FVC μετά βρογχοδιαστολή (± ΤΑ) | 0,5 (0,1) | 0,5 (0,1) |
| FEV1 πριν βρογχοδιαστολή (L) (± ΤΑ) | 1,3 (0,5) | 1,4 (0,5) |
| FEV1 μετά βρογχοδιαστολή (L) (± ΤΑ) | 1,4 (0,5) | 1,5 (0,5) |
| Προβλεπόμενο FEV1 μετά βρογχοδιαστολή (%) (± ΤΑ) | 50,6 (13,1) | 50,1 (12,6) |
| FEV1 <50% n (%) | 467 (49,7) | 478 (51,3) |
| SGRQ συνολικό (± ΤΑ) | 48,4 (17,4) | 51,5 (17,0) |
| E-RS:COPD συνολικό (± ΤΑ) | 12,9 (7,1) | 13,3 (7,0) |
| Δείκτης BODE (± ΤΑ) | 4,1 (1,7) | 4,0 (1,6) |
| FeNO (ppb) (± ΤΑ) | 24,3 (22,4) | 24,6 (26,0) |
| Ηωσινόφιλα – μέσος (κύτταρα/μL) (± ΤΑ) | 401 (298) | 407 (336) |
| Ηωσινόφιλα – διάμεσος (Q1–Q3) | 340 (240–460) | 330 (220–460) |
bΣτη μελέτη BOREAS, το 0,5% των συμμετεχόντων ήταν Μαύροι και το 14,3% ήταν Ασιάτες. Στη μελέτη NOTUS, το 1,3% των συμμετεχόντων ήταν Μαύροι και το 1,1% ήταν Ασιάτες.1
cΟι μέτριες παροξύνσεις ορίστηκαν ως παροξύνσεις που οδήγησαν σε θεραπεία με συστηματικά κορτικοστεροειδή, αντιβιοτικά ή και τα δύο.1
dΟι σοβαρές παροξύνσεις ορίστηκαν ως παροξύνσεις που οδήγησαν σε νοσηλεία ή παρακολούθηση για διάστημα άνω των 24 ωρών σε τμήμα επειγόντων περιστατικών ή μονάδα άμεσης φροντίδας.1
Ασφάλεια
Ασφάλεια BOREAS
| Ασφάλεια μελέτης BOREAS8,a | DUPIXENT (n=469) | Εικονικό φάρμακο (n=470) |
|---|---|---|
| Οποιαδήποτε ανεπιθύμητη ενέργεια (ΑΕ) | 77% | 76% |
| Οποιαδήποτε σοβαρή ανεπιθύμητη ενέργεια (ΣΑΕ) | 14% | 16% |
| Οποιαδήποτε ΑΕ που οδήγησε σε θάνατο | 2% | 2% |
| Οποιαδήποτε ΑΕ που οδήγησε σε μόνιμη διακοπή της μελέτης | 3% | 3% |
| Μείζον καρδιαγγειακόανεπιθύμητο συμβάνb | 1% | 1% |
| ΑΝΕΠΙΘΥΜΗΤΕΣ ΕΝΕΡΓΕΙΕΣ ΠΟΥ ΕΜΦΑΝΙΣΤΗΚΑΝ ΣΕ ≥5% ΤΩΝ ΑΣΘΕΝΩΝ ΣΕ ΟΠΟΙΑΔΗΠΟΤΕ ΟΜΑΔΑ | ||
| Ρινοφαρυγγίτιδα | 9% | 10% |
| Λοίμωξη του ανώτερου αναπνευστικού | 8% | 10% |
| Κεφαλαλγία | 8% | 7% |
| ΧΑΠ | 6% | 6% |
| COVID-19 | 4% | 6% |
| Υπέρταση | 4% | 6% |
| Διάρροια | 5% | 4% |
| Οσφυαλγία | 5% | 3% |
Ασφάλεια μελέτης NOTUS
|
Ασφάλεια NOTUS9,c |
DUPIXENT (n=469) |
Εικονικό φάρμακο (n=464) |
|---|---|---|
| Οποιαδήποτε ΑΕ | 67% | 66% |
| Οποιαδήποτε ΣΑΕ | 13% | 16% |
| Οποιαδήποτε ΑΕ με κατάληξη θάνατο | 3% | 2% |
| Οποιαδήποτε ΑΕ που οδήγησε σε μόνιμη διακοπή της μελέτης | 4% | 3% |
| Σημαντικό ανεπιθύμητο καρδιαγγειακόσυμβάνb | 1% | 2% |
| ΑΕ ΠΟΥ ΕΜΦΑΝΙΣΤΗΚΑΝ ΣΕ ≥5% ΤΩΝ ΑΣΘΕΝΩΝ ΣΕ ΟΠΟΙΑΔΗΠΟΤΕ ΟΜΑΔΑ | ||
| COVID-19 | 9% | 8% |
| Κεφαλαλγία | 8% | 7% |
| ΧΑΠ | 5% | 8% |
| Ρινοφαρυγγίτιδα | 6% | 5% |
Το DUPIXENT ΔΕΝ ΕΙΝΑΙ ΑΝΟΣΟΚΑΤΑΣΤΑΛΤΙΚΟ ΟΥΤΕ ΚΟΡΤΙΚΟΣΤΕΡΟΕΙΔΕΣ.1
ΑΠΟΔΕΔΕΙΓΜΕΝΟ ΠΡΟΦΙΛ ΑΣΦΑΛΕΙΑΣ ΣΕ 6 ΕΝΔΕΙΞΕΙΣ1
| Κατηγορία συστήματος | Ανεπιθύμητη ενέργεια | Συχνότηταd |
|---|---|---|
| Διαταραχές του αιμοποιητικού και λεμφικού συστήματος | Ηωσινοφιλία | Συχνή |
| Διαταραχές του ανοσοποιητικού συστήματος | Αγγειοοίδημαe | |
| Αναφυλακτική αντίδραση, αντίδραση ορονοσίας, αντίδραση ορονοσίας-όμοια | Όχι συχνή | |
| Σπάνια | ||
| Διαταραχές του δέρματος και του υποδόριου ιστού | Εξάνθημα προσώπουe | Όχι συχνή |
| Διαταραχές του μυοσκελετικού συστήματος και του συνδετικού ιστού | Αρθραλγίαe | Συχνή |
| Γενικές διαταραχές και καταστάσεις στη θέση χορήγησης | Αντιδράσεις στη θέση ένεσης (περιλαμβάνει ερύθημα, οίδημα, κνησμό, άλγος, διόγκωση και εκχυμώσεις) | Συχνή |
| Συχνές ανεπιθύμητες ενέργειες που εμφανίζονται κυρίως σε κλινικές δοκιμές ατοπικής δερματίτιδας | ||
| Λοιμώξεις και παρασιτώσεις | Επιπεφυκίτιδα, στοματικός έρπης | Συχνή |
| Διαταραχές οφθαλμών | Αλλεργική επιπεφυκίτιδα | Συχνή |
| Κερατίτιδα,e βλεφαρίτιδα,f κνησμός οφθαλμών,f ξηροφθαλμίαf | Όχι συχνή | |
| Ελκωτική κερατίτιδαe,f | Σπάνια | |
aΟ πληθυσμός ασφάλειας περιλάμβανε όλους τους ασθενείς που έλαβαν τουλάχιστον μία πλήρη ή μερική δόση του DUPIXENT ή εικονικού φαρμάκου· η ανάλυση πραγματοποιήθηκε σύμφωνα με τη θεραπεία που έλαβε κάθε ασθενής. Ένας ασθενής που είχε κατανεμηθεί στην ομάδα του εικονικού φαρμάκου έλαβε κατά λάθος DUPIXENT, επομένως ο πληθυσμός ασφάλειας περιλαμβάνει 470 ασθενείς στην ομάδα του εικονικού φαρμάκου και 469 ασθενείς στην ομάδα του DUPIXENT.8
bΣημαντικά ανεπιθύμητα καρδιαγγειακά συμβάντα (επιβεβαιωμένα) περιλάμβαναν θάνατο λόγω καρδιαγγειακών αιτίων, μη θανατηφόρο έμφραγμα του μυοκαρδίου και μη θανατηφόρο εγκεφαλικό επεισόδιο.8,9
cΟ πληθυσμός ασφάλειας περιλάμβανε όλους τους ασθενείς που έλαβαν τουλάχιστον μία πλήρη ή μερική δόση του DUPIXENT ή εικονικού φαρμάκου· η ανάλυση πραγματοποιήθηκε σύμφωνα με τη θεραπεία που έλαβε κάθε ασθενής.9
dΣυχνές (≥1/100 έως <1/10)· όχι συχνές (≥1/1000 έως <1/100)· σπάνιες (≥1/10.000 έως <1/1000).1
eΑπό αναφορές μετά την κυκλοφορία.1
fΟι συχνότητες για τον κνησμό οφθαλμών, τη βλεφαρίτιδα και την ξηροφθαλμία ήταν συχνές, ενώ η ελκωτική κερατίτιδα ήταν όχι συχνή στις μελέτες ατοπικής δερματίτιδας.1
Δοσολογία
Η ΕΥΕΛΙΞΙΑ ΤΗΣ ΧΟΡΗΓΗΣΗΣ ΣΤΟ ΣΠΙΤΙ Ή ΣΤΟ ΙΑΤΡΕΙΟ

a300 mg=2 mL διάλυμα.1

DUPIXENT Προγεμισμένη Πένα1
Αυτόματος εγχυτήρας με μία πίεση
Διαδικασία δύο σαφών βημάτων
Οπτική και ηχητική επιβεβαίωση
Συμπαγής και πρακτική στη μεταφορά
Κρυμμένη βελόνα
Το DUPIXENT προορίζεται για χρήση υπό την καθοδήγηση επαγγελματία υγείας1
-
Το DUPIXENT μπορεί να χορηγηθεί από τον ασθενή ή τον φροντιστή στο σπίτι, μετά από εκπαίδευση στην τεχνική υποδόριας ένεσης με τη χρήση αυτόματης συσκευής ένεσης (για ενήλικες και εφήβους) ή προγεμισμένης σύριγγας
-
Οι ιατροί ή οι νοσηλευτές θα πρέπει να παρέχουν κατάλληλη εκπαίδευση στους ασθενείς και/ή στους φροντιστές σχετικά με την προετοιμασία και τη χορήγηση του DUPIXENT πριν από τη χρήση, σύμφωνα με τις Οδηγίες Χρήσης
-
Το DUPIXENT μπορεί να χορηγηθεί στο ιατρείο υπό την καθοδήγηση επαγγελματία υγείας, εάν ο ασθενής ή ο φροντιστής δεν είναι κατάλληλος για αυτοχορήγηση της ένεσης
Για πλήρεις οδηγίες χορήγησης, παρακαλούμε πατήστε εδώ για την ΠΧΠ.
Το Dupixent είναι εγκεκριμένο για1
Ατοπική δερματίτιδα

μη ελεγχόμενη σοβαρήb
Άσθμα

σοβαρό άσθμα τύπου 2 ή εξαρτώμενο από ΟΚΣ-cc
Χρόνια ρινοκολπίτιδα με ρινικούς πολύποδες

σοβαρή, ανεπαρκώς ελεγχόμενη
Οζώδης κνήφη

μη ελεγχόμενη, μέτρια έως σοβαρή
Ηωσινοφιλική οισοφαγίτιδα

ανεπαρκώς ελεγχόμενη
ΧΑΠ

μη ελεγχόμενη παρά τη βέλτιστη εισπνεόμενη θεραπείαd
ΑΤΟΠΙΚΗ ΔΕΡΜΑΤΙΤΙΔΑ
Το DUPIXENT ενδείκνυται για τη θεραπεία της μέτριας έως σοβαρής ατοπικής δερματίτιδας σε ενήλικες και εφήβους ηλικίας 12 ετών και άνω που είναι υποψήφιοι για συστηματική θεραπεία.
Το DUPIXENT ενδείκνυται για τη θεραπεία της σοβαρής ατοπικής δερματίτιδας σε παιδιά ηλικίας από 6 μηνών έως 11 ετών που είναι υποψήφιοι για συστηματική θεραπεία.
ΑΣΘΜΑ
Το Dupixent ενδείκνυται σε ενήλικες και εφήβους ηλικίας 12 ετών και άνω ως πρόσθετη θεραπεία συντήρησης για το σοβαρό άσθμα με φλεγμονή τύπου 2 που χαρακτηρίζεται από αυξημένο αριθμό 3 ηωσινοφίλων στο αίμα και/ή αυξημένα επίπεδα κλάσματος εκπνεόμενου μονοξειδίου του αζώτου (FeNO), οι οποίοι δεν ελέγχονται επαρκώς με υψηλής δόσης εισπνεόμενα κορτικοστεροειδή (ICS) σε συνδυασμό με ένα άλλο φαρμακευτικό προϊόν για θεραπεία συντήρησης.
Το Dupixent ενδείκνυται σε παιδιά ηλικίας 6 έως 11 ετών ως πρόσθετη θεραπεία συντήρησης για το σοβαρό άσθμα με φλεγμονή τύπου 2 που χαρακτηρίζεται από αυξημένο αριθμό ηωσινοφίλων στο αίμα και/ή αυξημένα επίπεδα κλάσματος εκπνεόμενου μονοξειδίου του αζώτου (FeNO), τα οποία δεν ελέγχονται επαρκώς με μέτριας έως υψηλής δόσης εισπνεόμενων κορτικοστεροειδών (ICS) σε συνδυασμό με ένα άλλο φαρμακευτικό προϊόν για θεραπεία συντήρησης.
ΧΡΟΝΙΑ ΡΙΝΟΚΟΛΠΙΤΙΔΑ ΜΕ ΡΙΝΙΚΟΥΣ ΠΟΛΥΠΟΔΕΣ (CRSwNP)
Το Dupixent ενδείκνυται ως πρόσθετη θεραπεία σε συνδυασμό με ενδορρινικά κορτικοστεροειδή για τη θεραπεία ενηλίκων με σοβαρή CRSwNP στους οποίους η θεραπεία με συστηματικά κορτικοστεροειδή και/ή χειρουργική επέμβαση δεν παρέχει επαρκή έλεγχο της νόσου.
ΟΖΩΔΗΣ ΚΝΗΦΗ (PN)
Το DUPIXENT ενδείκνυται για τη θεραπεία ενηλίκων με μέτρια έως σοβαρή οζώδη κνήφη που είναι υποψήφιοι για συστηματική θεραπεία.
ΗΩΣΙΝΟΦΙΛΙΚΗ ΟΙΣΟΦΑΓΙΤΙΔΑ (EoE)
Το Dupixent ενδείκνυται για τη θεραπεία της ηωσινοφιλικής οισοφαγίτιδας σε ενήλικες, εφήβους και παιδιά ηλικίας 1 έτους και άνω με σωματικό βάρος τουλάχιστον 15 kg, οι οποίοι δεν ελέγχονται επαρκώς, έχουν δυσανεξία ή δεν είναι υποψήφιοι για συμβατική φαρμακευτική θεραπεία.
ΧΡΟΝΙΑ ΑΠΟΦΡΑΚΤΙΚΗ ΠΝΕΥΜΟΝΟΠΑΘΕΙΑ (ΧΑΠ)
Το Dupixent ενδείκνυται σε ενήλικες ως πρόσθετη θεραπεία συντήρησης για τη μη ελεγχόμενη χρόνια αποφρακτική πνευμονοπάθεια (ΧΑΠ) που χαρακτηρίζεται από αυξημένο αριθμό ηωσινοφίλων στο αίμα σε συνδυασμό με ένα εισπνεόμενο κορτικοστεροειδές (ICS), έναν β2-αγωνιστή μακράς δράσης (LABA) και έναν μουσκαρινικό ανταγωνιστή μακράς δράσης (LAMA), ή σε συνδυασμό με έναν LABA και έναν LAMA εάν το ICS δεν ενδείκνυται
aΑπό την αρχική έγκριση από τον FDA για ασθενείς με ατοπική δερματίτιδα, άσθμα, χρόνια ρινοκολπίτιδα με ρινικούς πολύποδες, οζώδη κνησμό, EoEκαι ΧΑΠ.15
bΣε ασθενείς ηλικίας από 6 μηνών έως 11 ετών. Το DUPIXENT ενδείκνυται για μέτρια έως σοβαρή ατοπική δερματίτιδα σε ασθενείς ηλικίας 12 ετών και άνω.1
cΕξαρτώμενοι από συστηματικά κορτικοστεροειδή, όπως ορίζεται στις κατευθυντήριες οδηγίες GINA.15
dΤριπλή εισπνεόμενη θεραπεία ή διπλή εισπνεόμενη θεραπεία εάν τα εισπνεόμενα κορτικοστεροειδή δεν είναι κατάλληλα.1
AE, ανεπιθύμητο συμβάν
BD, βρογχοδιασταλτικό
BL, βασική γραμμή
BODE, δείκτης μάζας σώματος, απόφραξη αεραγωγών, δύσπνοια και ικανότητα άσκησης
ΧΑΠ, χρόνια αποφρακτική πνευμονοπάθεια
CRS, χρόνια ρινική ιγμορίτιδα
EoE, ηωσινοφιλική οισοφαγίτιδα
EOS, ηωσινόφιλο
E-RS: COPD, Αξιολόγηση Αναπνευστικών Συμπτωμάτων στη ΧΑΠ
EXACT, Εργαλείο Αξιολόγησης Παροξύνσεων στη ΧΑΠ
FeNO, κλασματικό εκπνεόμενο μονοξείδιο του αζώτου
FEV1, αναγκαστικός εκπνεόμενος όγκος σε 1 δευτερόλεπτο
FVC, αναγκαστική ζωτική χωρητικότητα
GINA, Παγκόσμια Πρωτοβουλία για το Άσθμα
GOLD, Παγκόσμια Πρωτοβουλία για τη Χρόνια Αποφρακτική Πνευμονοπάθεια
ICS, εισπνεόμενο κορτικοστεροειδές
ICU, μονάδα εντατικής θεραπείας
LABA, μακράς δράσης βήτα αγωνιστής
LAMA, μακράς δράσης μουσκαρινικός ανταγωνιστής
LSM, μέση τιμή ελαχίστων τετραγώνων
mMRC, Τροποποιημένο Ιατρικό Συμβούλιο Έρευνας
OCS, από του στόματος κορτικοστεροειδές
OR, λόγος πιθανοτήτων
Q2W, μία φορά κάθε 2 εβδομάδες
SAE, σοβαρό ανεπιθύμητο συμβάν
SC, υποδόρια
SGRQ, Ερωτηματολόγιο Αναπνευστικής Λειτουργίας St George
SOC, συνήθης θεραπευτική αγωγή
Μπορείτε να βρείτε την Περίληψη Χαρακτηριστικών του Προϊόντος πατώντας εδώ.
Πριν τη συνταγογράφηση συμβουλευτείτε την περίληψη χαρακτηριστικών του προϊόντος
Τρόπος διάθεσης: Περιορισμένη ιατρική συνταγή από ειδικό ιατρό λόγω ανάγκης παρακολούθησης κατά τη διάρκεια της αγωγής.
| ΠΡΟΪΟΝ | Λ.Τ. |
| BTx2 PF.SYRS 200mg | 1162,26 € |
| BTx2 PF.SYRS 300mg | 1158,38 € |
| BTx2 PF.PENS 200mg | 1163,00 € |
| BTx2 PF.PENS 300mg | 1163,00 € |
.png)
Αναφορές:
1. Περίληψη Χαρακτηριστικών του Προϊόντος DUPIXENT.
2. Garudadri S, Woodruff PG. Targeting chronic obstructive pulmonary disease phenotypes, endotypes, and biomarkers. Ann Am Thorac Soc. 2018;15(suppl 4): S234-S238. doi:10.1513/AnnalsATS.201808-533MG
3. Gandhi NA, Bennett BL, Graham NMH, Pirozzi G, Stahl N, Yancopoulos GD. Targeting key proximal drivers of type 2 inflammation in disease. Nat Rev Drug Discov. 2016;15(1):35-50. doi:10.1038/nrd4624
4. Rabe KF, Rennard S, Martinez FJ, et al. Targeting type 2 inflammation and epithelial alarmins in chronic obstructive pulmonary disease: a biologics outlook. Am J Respir Crit Care Med. 2023;208(4):395-405. doi:10.1164/rccm.202303-0455CI
5. Saatian B, Rezaee F, Desando S, et al. Interleukin-4 and interleukin-13 cause barrier dysfunction in human epithelial cells. Tissue Barriers. 2013;1(2): e24333. doi:10.4161/tisb.24333
6. Cooper PR, Poll CT, Barnes PJ, Sturton RG. Involvement of IL-13 in tobacco smoke–induced changes in the structure and function of rat intrapulmonary airways. Am J Respir Cell Mol Biol. 2010;43(2):220-226. doi:10.1165/rcmb.2009-0117OC
7. Global Initiative for Chronic Obstructive Lung Disease. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease (2024 report). Accessed December 18, 2025. https://goldcopd.org/2024-gold-report/
8. Bhatt SP, Rabe KF, Hanania NA, et al; BOREAS Investigators. Dupilumab for COPD with type 2 inflammation indicated by eosinophil counts. N Engl J Med. 2023;389(3):205-214. doi:10.1056/NEJMoa2303951
9. Bhatt SP, Rabe KF, Hanania NA, et al; NOTUS Study Investigators. Dupilumab for COPD with blood eosinophil evidence of type 2 inflammation. N Engl J Med. 2024;390(24):2274-2283. doi:
10.1056/NEJMoa2401304 10. Suissa S, Dell’Aniello S, Ernst P. Long-term natural history _of chronic obstructive pulmonary disease: severe exacerbations and mortality. Thorax. 2012;67(11):957-963. doi:10.1136/thoraxjnl-2011-201518
11. Jones PW. St George’s Respiratory Questionnaire Manual. Version 2.4, March 2022. Accessed February 05, 2026 SGRQ-Manual-March-2022.pdf
12. EXACT and E-RS: COPD content. Evidera website. Accessed December 18, 2025. https://www.evidera.com/what-we-do/patient-centered-research/coa-instrument-management-services/exact-program/exact-content/
13. Leidy NK, Bushnell DM, Thach C, Hache C, Gutzwiller FS. Interpreting Evaluating Respiratory Symptoms™ in COPD diary scores in clinical trials: terminology, methods, and recommendations. Chronic Obstr Pulm Dis. 2022;9(4):576-590. doi:10.15326/ jcopdf.2022.0307
14. Bushnell DM, Wilson R, Gutzwiller FS, et al. Use of the Evaluating Respiratory Symptoms™ in COPD as an outcome measure in clinical trials: a rapid systematic review. Chronic Obstr Pulm Dis. 2021;8(4):551-571. doi:10.15326/jcopdf.2021.0235
15. Global Initiative for Asthma. Global strategy for asthma management and prevention. Updated 2024. Accessed December 18, 2025. https://ginasthma.org/wp-content/uploads/2024/05/GINA-2024-Strategy-Report-24_05_22_WMS.pdf

© 2024 Sanofi και Regeneron Pharmaceuticals, Inc. Με την επιφύλαξη παντός δικαιώματος.
MAT-GR-2500549, v1.0, 03/2026