FLUZONEMD Trivalent
Pour les patients âgés de 6 mois et plus

Une option de vaccin trivalent contre la grippe pour les enfants et les adultes*
Le vaccin FLUZONEMD Trivalent contre les types A et B du virus de la grippe (à virion fragmenté) est indiqué pour l’immunisation active contre la grippe causée par les souches spécifiques du virus de la grippe contenues dans le vaccin, chez les adultes et les enfants de 6 mois et plus.1
À propos de FLUZONEMD Trivalent
FLUZONEMD Trivalent est un vaccin contre le virus de la grippe inactivé à virion fragmenté qui consiste en une suspension stérile contenant trois souches de virus de la grippe cultivées dans des œufs de poule embryonnés.*
Formes posologiques et ingrédients*

FLUZONEMD Trivalent est fourni dans des seringues préremplies contenant une seule dose et dans des fioles multidoses.
Le vaccin est disponible en emballages de :
- 1 fiole de 5 mL (multidose)
- 10 seringues de 0,5 mL (dose unique) sans aiguille

Ce vaccin est conforme aux recommandations de l’Organisation mondiale de la Santé (OMS) pour la saison de la grippe 2025-2026 (hémisphère nord).
E Chaque dose de 0,5 mL est formulée pour contenir 15 µg d’hémagglutinine (HA) pour chacune des souches indiquées ci-dessous.
A (H3N2)
A (H1N1)
B/souche
Ingrédients non médicinaux :
Dose de 0,5 mL
Solution saline tamponnée au phosphate [chlorure de sodium 6,51 g/L; phosphate de sodium (dibasique anhydre) 3,83 g/L; phosphate de sodium (monobasique anhydre) 0,410 g/L]
Quantité d’eau pour injection suffisante jusqu’à 0,5 mL
≤ 250 μg TritonMD X-100
0,01 % de thimérosal p/v dans les présentations multidoses seulement
* La signification clinique n’a pas été établie.
Posologie et administration
Patients âgés de 6 mois à 35 mois
1 ou 2 dosesa,
à 4 semaines d’intervalleb 0,25 mLc ou 0,5 mLd
Patients âgés de 3 à 8 ans
1 ou 2 dosesa 0,5 mL
Patients âgés de 9 ans et plus
1 dose 0,5 mL
REMARQUE : les doses fractionnées (doses de moins de volume que celles indiquées ci-dessus pour chaque groupe d’âge) ne doivent pas être administrées.
a Les enfants âgés de 6 mois à moins de 9 ans n’ayant pas été vaccinés auparavant ont besoin de 2 doses du vaccin contre l’influenza saisonnière à un intervalle de 4 semaines. Il est recommandé que les enfants admissibles âgés de moins de 9 ans qui ont bien reçu une ou plusieurs doses du vaccin contre l’influenza saisonnière dans le passé reçoivent une dose par saison les années suivantes.
b Si la deuxième dose de l’enfant a été oubliée, celle-ci peut être administrée à tout moment.
c Dans les études cliniques, les enfants âgés de 6 mois à 35 mois ont reçu une dose de 0,25 mL.
d Le CCNI préconise l’administration d’une dose complète de 0,5 mL de vaccin antigrippal aux enfants âgés de 6 mois à 35 mois.
Étapes pour l’injection
- Ne pas administrer par injection intravasculaire. Administrer le vaccin par voie intramusculaire.
- FLUZONEMD Trivalent ne doit pas être administré dans une fesse. Le point d’injection à privilégier est le muscle deltoïde chez les adultes et les nourrissons de moins d’un an et dans la partie antérolatérale du milieu de la cuisse chez les nourrissons de moins d’un an.
- Avant d’administrer chaque dose, bien agiter le flacon et la seringue préremplie.
- Utiliser une technique aseptique. Utiliser une aiguille et une seringue stériles distinctes (ou une seringue stérile préremplie) pour chaque patient et à chaque utilisation de la fiole multidose. Ne pas remettre les capuchons sur les aiguilles, et se débarrasser de ces dernières conformément aux lignes directrices applicables aux déchets biologiques dangereux.
- Remettre au patient un carnet de vaccination personnel permanent. De plus, il est essentiel que le médecin ou le personnel infirmier inscrive les antécédents d’immunisation dans le dossier médical permanent de chaque patient. Cela doit contenir le nom du vaccin, la date de son administration, la dose, le fabricant et le numéro du lot.
Profil d’innocuité
Les souches des vaccins contre le virus de l’influenza sont sujettes à des changements annuels. Les études cliniques respectives, y compris chez au moins 50 adultes âgés de 18 à 60 ans et chez au moins 50 adultes âgés de 60 ans ou plus, sont menées afin d’évaluer l’innocuité et l’immunogénicité de FLUZONEMD. Aux fins de l’analyse cumulative, cinq années de données d’innocuité cliniques sont présentées ci-dessous. Dans cet ensemble de données, un total de 601 personnes vaccinées ont reçu une injection intramusculaire de FLUZONEMD.
Pourcentage des réactions au site d’injection et événements systémiques indésirables sollicités chez les enfants et les adultes suivant la vaccination avec FLUZONEMD Trivalent
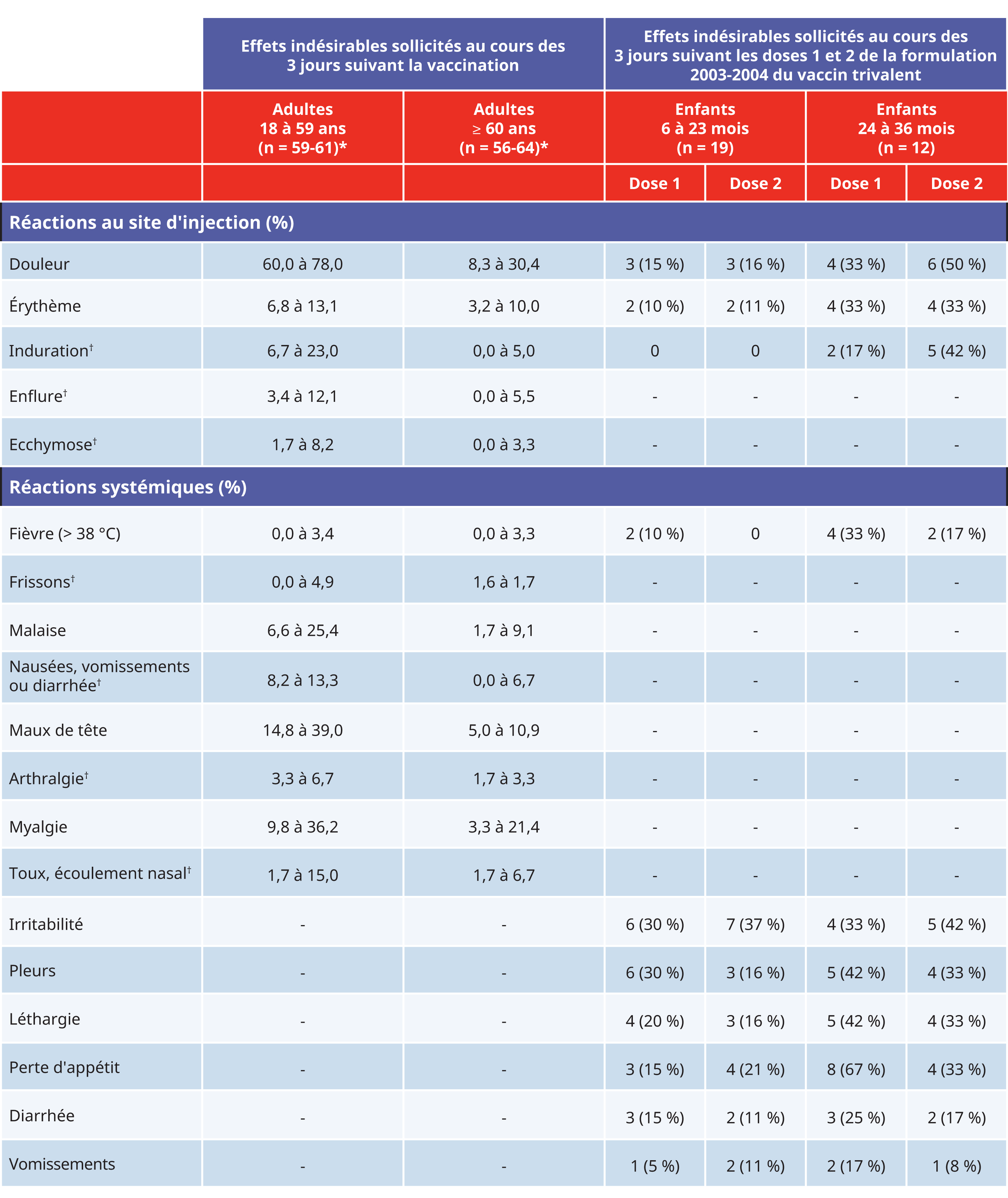
* population pour l’évaluation de l’innocuité analysée par étude
† les effets indésirables spécifiques n’ont pas été déclarés ou sollicités dans toutes les études
Renseignements relatifs à l’innocuité
CONTRE-INDICATIONS :
Ne doit pas être administré à une personne ayant des antécédents de réactions allergiques graves aux protéines d’œuf ou à tout composant du vaccin, ou ayant déjà reçu une dose du vaccin ou un vaccin contenant les mêmes composants ou constituants.
USAGE CLINIQUE :
- Enfants (âgés de 6 mois à 18 ans) : d’après les données présentées et examinées par Santé Canada, l’innocuité et l’efficacité de FLUZONEMD chez les patients pédiatriques ont été démontrées. Par conséquent, Santé Canada a autorisé une indication d’utilisation dans la population pédiatrique.
- L’innocuité et l’efficacité de l’administration de FLUZONEMD chez les enfants de moins de 6 mois n’ont pas été établies.
- Personnes âgées : les données probantes tirées des études cliniques et de l’expérience suggèrent que l’utilisation dans la population gériatrique est associée à des différences en matière de sécurité ou d’efficacité.
MISES EN GARDE ET PRÉCAUTIONS PERTINENTES :
- Ne pas administrer par injection intravasculaire. Ne pas administrer dans une fesse.
- Comme c’est le cas avec tout vaccin, il est possible que l’immunisation avec FLUZONEMD Trivalent ne protège pas 100 % des personnes.
- Il convient de reporter la vaccination en cas de maladie aiguë modérée ou sévère avec ou sans fièvre : cependant, en cas de maladie légère accompagnée d’une faible fièvre, le vaccin pourrait être administré.
- FLUZONEMD Trivalent ne devrait pas être administré aux personnes présentant un trouble hémorragique tel que l’hémophilie ou la thrombocytopénie, ou aux personnes qui prennent un anticoagulant, sauf si les avantages potentiels de la vaccination l’emportent sur le risque qu’elle représente. Si la décision est prise d’administrer un produit par injection intramusculaire à ces personnes, il faut le faire avec précaution, en respectant des étapes afin d’éviter tout risque de formation d’hématome après l’injection.
- Il se peut que les personnes immunocompromises n’obtiennent pas la réponse immunitaire attendue.
- L’immunisation doit être différée chez un patient souffrant d’un trouble neurologique évolutif, mais doit être envisagée lorsque le processus de la maladie a été stabilisé.
- Le syndrome de Guillain-Barré (SGB) a été signalé après la vaccination antigrippale. Cependant, on ne sait pas si la vaccination antigrippale pourrait spécifiquement augmenter le risque de récidive du SGB. Par conséquent, le CCNI et le Comité consultatif sur les pratiques d’immunisation (Advisory Committee on Immunization Practices, ACIP) des États-Unis recommandent qu’il est prudent d’éviter de vacciner les personnes qui ne présentent pas un risque élevé de complications sévères liées à la grippe et qui ont déjà présenté un SGB dans les six semaines suivant une vaccination antigrippale.
- Une syncope peut survenir après, ou même avant, l’administration de n’importe quel vaccin. Il s’agit d’une réaction psychogène à une injection à l’aide d’une aiguille. Il importe que des mesures soient mises en place afin de prévenir les chutes et les blessures et d’aider à la prise en charge des syncopes.
-
Aucune étude sur la reproduction animale n’a été effectuée avec FLUZONEMD. On ne sait pas non plus si FLUZONEMD peut nuire au fœtus lorsqu’il est administré à une femme enceinte ou s’il peut affecter la capacité de reproduction. Les données sur l’utilisation de ce vaccin chez des femmes enceintes sont limitées. FLUZONEMD ne doit être administré à une femme enceinte que si cela est manifestement nécessaire et seulement après l’évaluation des risques et des bienfaits. Il n’existe cependant aucune preuve suggérant un risque pour le fœtus ou la grossesse suite à la vaccination de la mère avec FLUZONEMD. Le CCNI affirme que la vaccination antigrippale est recommandée pour les femmes enceintes.
- On ne dispose d’aucune donnée sur la présence de FLUZONEMD Trivalent dans le lait maternel humain, sur les effets sur la production de lait ou sur le nourrisson allaité. Aucune conclusion ne peut être tirée quant à savoir si FLUZONEMD Trivalent peut être utilisé sans danger pendant l’allaitement. FLUZONEMD Trivalent ne doit être utilisé pendant l’allaitement que si les bienfaits potentiels pour la mère l’emportent sur les risques, y compris les risques pour l’enfant nourri au sein. Le CCNI indique que la vaccination contre l’influenza est considérée comme sécuritaire pour les femmes qui allaitent.
POUR DE PLUS AMPLES RENSEIGNEMENTS :
Veuillez consulter la Monographie du Produit pour obtenir des renseignements importants qui n’ont pas été discutés dans ce document en ce qui concerne les effets indésirables, les interactions médicamenteuses et la posologie. Il est aussi possible d’obtenir la Monographie du Produit auprès de notre service médical.
Appelez-nous au 1-800-265-7927.
- Monographie de produit : FLUZONEMD Trivalent. Sanofi Pasteur. 13 février 2025.
- Une déclaration d’un comité consultatif (DCC)/Comité consultatif national de l’immunisation (CCNI) : Chapitre sur la grippe du Guide canadien d’immunisation et Déclaration sur la vaccination antigrippale pour la saison 2024–2025. Mai 2024.
MAT-CA-2500261-v.2 09/2025


.jpg/jcr:content/image%20(2).jpg)
.jpg/jcr:content/image%20(3).jpg)
.jpg/jcr:content/image%20(1).jpg)