NDMM
Mieloma Múltiplo recém diagnosticado (de novo)
REGIMES DE 1ª LINHA FINANCIADOS PELO SNS1-10
*VRd - Não financiado mas extensamente utilizado. a V interrompido após 8º ciclos
Não podem ser estabelecidas conclusões da comparação directa de estudos clínicos uma vez que os desenhos de estudos e população incluída podem ser diferentes.
RRMM
Mieloma Múltiplo recidivante e/ou refratário
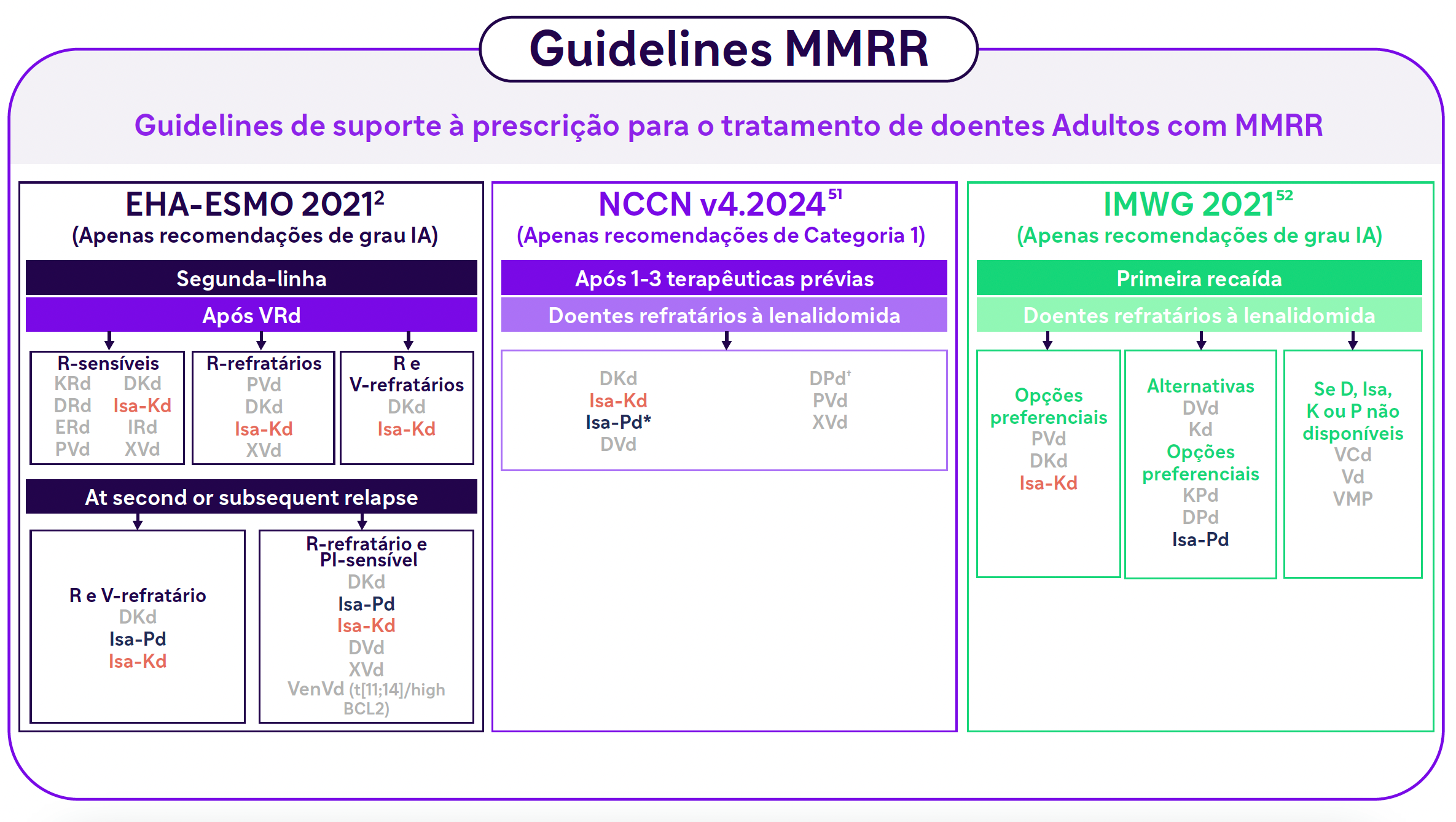
REGIMES DE 2ª LINHA FINANCIADOS PELO SNS13-31
2L
PFS
Características na baseline
ITT
2L
Len-ref
Len-ref
ldade
mediana
mediana
Mediana
Nº prévio
de linhas
Nº prévio
de linhas
11,2
meses
meses
17,8
meses
meses
9,5
meses
meses
71%
67
2
16.7
meses
meses
27
meses
meses
7,8
meses
meses
24%
64
2
11,1 meses
Não
incluíu
incluíu
11,4
meses
meses
94%
68
3
Não
atingido
atingido
Não
atingido
atingido
9,0
meses
meses
73%
70
2
35,7
meses
meses
38,2
meses
meses
HR=0,6
32%
65
2
18,7
meses
meses
22,2
meses
meses
8,6
meses
meses
24%
65
2
IKEMA
Isa-Kd está financiado pelo SNS para utilização em doentes que
tenham recebido pelo menos uma terapêutica anterior14
tenham recebido pelo menos uma terapêutica anterior14
Isa-Kd demonstrou uma mPFS sem precedentes de 35,7 meses.
A maior mPFS observada num estudo de Fase III em que se avaliou a combinação
de um Anti-CD38 + PI e que incluiu doentes refratários à lenalidomida27,31-50
A maior mPFS observada num estudo de Fase III em que se avaliou a combinação
de um Anti-CD38 + PI e que incluiu doentes refratários à lenalidomida27,31-50
ICARIA
Isa-Pd está financiado pelo SNS para utilização em doentes refratários
à lenalidomida e expostos a um PI em 1ª linha de tratamento15
à lenalidomida e expostos a um PI em 1ª linha de tratamento15
Isa-Pd é a única combinação 2L com anti-CD38 livre de lenalidomida (R) e IP com PFS de 11,4 meses em doentes len-ref e uma PFS 2L não atingida aos 14,2 meses de follow-up.13-31
- Resumo das Características do Medicamento. Sanofi Produtos Farmacêuticos Portugal, Fevereiro 2025
- Dimopoulos MA, Moreau P, Terpos E, et al. Multiple myeloma: EHA-ESMO clinical practice guidelines for diagnosis, treatment and follow-up. Ann Oncol. 2021;32(3):309-322
- Orientações CNFT VCd, 11/12/2021, CNFT MdS
- Relatório Público de Avaliação DVTd, 12/04/2022, INFARMED
- Relatório de Avaliação Pública Rd, 14/07/2020, INFARMED
- Relatório de Avaliação Pública Rd, 10/12/2021, INFARMED
- Relatório de Avaliação Pública DRd, 28/03/2022, INFARMED
- Relatório de Avaliação Pública VMP, 04/12/2017, INFARMED
- Relatório de Avaliação Pública DVMP, 28/03/2022, INFARMED
- REF-308090
- Lecat CSY, et al. Front Oncol. 2021;11:703233;
- Durie BGM, et al. Lancet. 2017;389(10068):519-27.
- Decaux O, et al. Eur J Haematol. 2024 May 7. doi:10.1111/ejh.14225. PMID: 38712850.
- Relatório Publico IsaKd, xx/xx/2025, INFARMED
- Relatório Publico IsaPd, 27/01/2022, INFARMED
- Relatório de Avaliação Pública PVd, 26/03/2024, INFARMED
- Relatório de Avaliação Pública DVd, 22/03/2019, INFARMED
- Relatório de Avaliação Pública Kd, 15/07/2020, INFARMED
- Relatório de Avaliação Pública KRd, 01/10/2018, INFARMED
- Relatório de Avaliação Pública IxaRd, 16/07/2019,INFARMED
- Relatório de Avaliação Pública Rd, 30/01/2009,INFARMED
- Relatório de Avaliação Pública DRd, 28/12/2018,INFARMED
- Richardson PG, et al. Lancet Oncol. 2019;20:781–94; 8.
- Weisel K, et al, ASH 2019, poster 3192
- Richardson, P. G., et al. The Lancet Oncology, 23(3), 416-427.
- Bringhen S, et al. Leuk Res 2021;104:106576
- Martin T, et al. Blood Cancer J. 2023;13(1):72. doi:10.1038/s41408-023-00797-8.
- Dimopoulos MA, et al. Lancet Oncol 2016;17:27–38;
- Dimopoulos MA, et al. Lancet Oncol 2017;18:1327–37
- Moreau P, et al. Leukemia. 2017 Jan;31(1):115-122.
- Hernández-Rivas JÁ, et al. Biomark Res. 2022;10(1):1–23.
- Spicka I, et al. Ann Hematol. 2019;98(9):2139–2150.
- Usmani SZ, et al. Lancet Oncol. 2022;23(1):65–76.
- Schjesvold FH, et al. Lancet Haematol. 2022;9(2):e98–e110.
- Du J, et al. Int J Hematol. 2021;113(3):422–429.
- Terpos E, et al. Eur J Haematol. 2018;100(1):10–18.
- Dimopoulos M, et al. Lancet Oncol. 2013;14(11):1129–1140.
- Dimopoulos MA, et al. Blood. 2016;128(4):497–503.
- Usmani SZ, et al. Haematologica. 2022;107(10):2408–2417.
- ClinicalTrials.gov. NCT01324947. Updated Nov 19, 2019. Accessed Jun 16, 2022.
- Janssen R&D. Clinical study report: VELCADE® + dexamethasone in RRMM. Apr 23, 2019. Accessed Jun 6, 2022.
- Hájek R, et al. Leukemia. 2017;31(1):107–114.
- Kropff M, et al. Haematologica. 2012;97(5):784–791.
- Usmani SZ, et al. Lancet Haematol. 2020;7(6):e447–e455.
- Lonial S, et al. Lancet Oncol. 2020;21(2):207–221.
- Bahlis NJ, et al. Leukemia. 2020;34(7):1875–1884.
- GSK. DREAMM-3 update press release. Nov 7, 2022. https://www.gsk.com
- Fu W, et al. Clin Lymphoma Myeloma Leuk. 2023;23(1):e51–e58.
- Moreau P, et al. N Engl J Med. 2022;387(6):495–505.
- Rodriguez-Otero P, et al. N Engl J Med. 2023;388(11):1002–1014.
- NCCN guidelines v4.2024;
- Moreau P, et al. Lancet 2021;22:e105-18
MAT-PT-2500478 | Julho 2025
Para continuar a ler confirme que é um profissional de saúde