- Article
- Source: Campus Sanofi
Docetaxel trong đIều trị bổ trợ ung thư vú her2 (+) vớI phác đồ hóa trị không chứa anthracycline - ca lâm sàng
.png/jcr:content/1920%20X%20565%20(51).png)
.png)
Khám lâm sàng:
- Toàn trạng ổn định.
- Nhịp tim đều rõ, không thấy tiếng thổi bệnh lý.
- Tại chỗ: U 1/4 trên ngoài vú phải kích thước ~ 2 cm, cứng chắc, ranh giới không rõ, mặt gồ ghề, di động dễ. Vú đối bên không thấy gì đặc biệt. Hạch nách 2 bên không sờ thấy, hạch nơi khác không sờ thấy.
- Các bộ phận khác chưa thấy gì đặc biệt.
Cận lâm sàng:
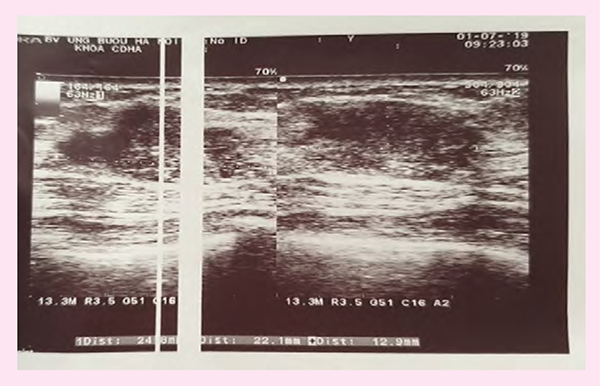
- Siêu âm tuyến vú: U vị trí 1/4 trên ngoài vú phải, không xâm lấn da, chưa dính cơ ngực lớn, kt: 22x13 mm, không thấy hạch nách.
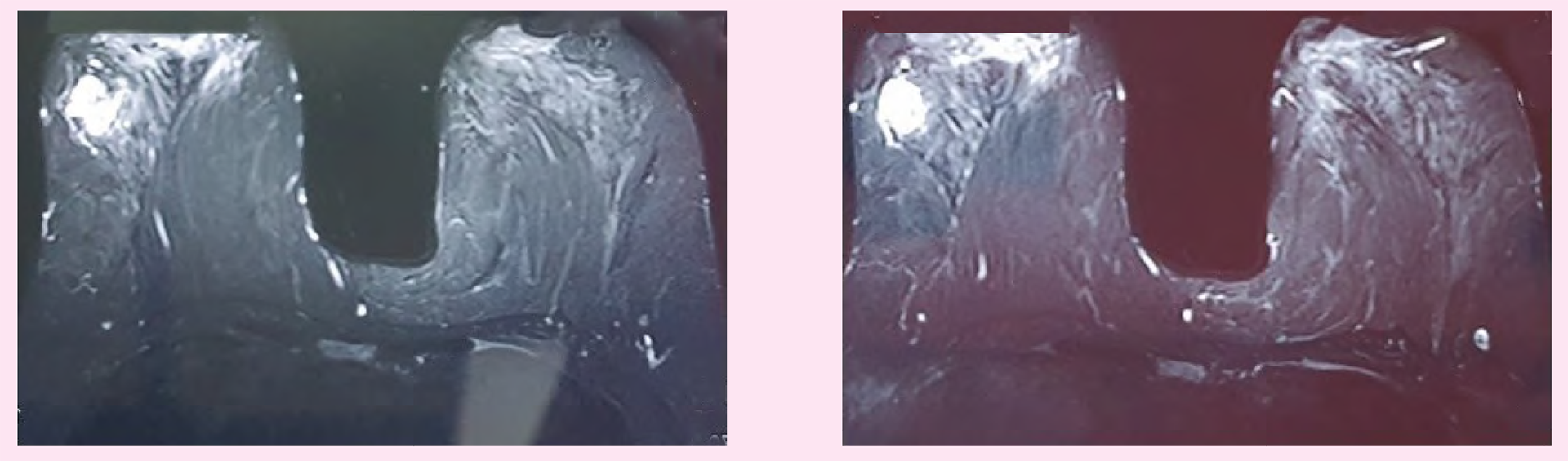
- Chụp cộng hưởng từ (MRI) vú: U vú phải 1/4 trên ngoài kích thước ~ 16x20 mm, không thâm nhiễm da và cơ ngực. Hố nách 2 bên không thấy hạch.
- Chọc hút tế bào bằng kim nhỏ u vú phải: ung thư biểu mô tuyến vú.
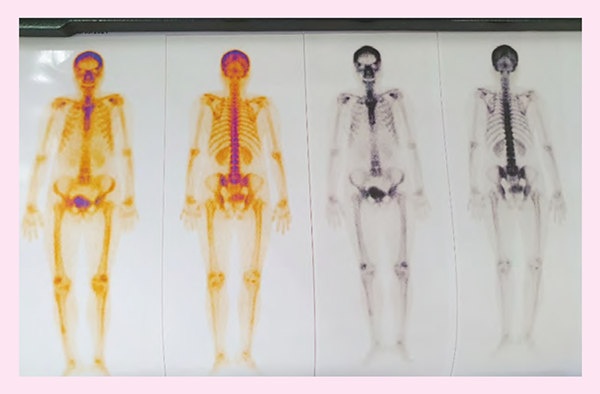
- Siêu âm tim: HHoHL nhẹ, EF: 73% y Các xét nghiệm khác chưa phát hiện bất thường (MRI sọ não, xạ hình xương bình thường).
Chẩn đoán trước mổ:
Ung thư vú phải cT2N0M0 – Giai đoạn IIA
ĐIều trị:
- Bệnh nhân đã được phẫu thuật cắt tuyến vú phải + vét hạch nách phải
- Sau mổ ổn định, vết mổ khô.
- Giải phẫu bệnh sau mổ: Ung thư biểu mô thể ống xâm nhập độ II, u kích thước 2 x 1,8x1,5 cm, 12/12 hạch âm tính
- Hóa mô miễn dịch: ER (+++) 90%, PR (+++) 90%, HER2(+++) 90%, Ki67 (+) 15%
- Chẩn đoán sau mổ: Ung thư vú phải pT2N0M0
- Hướng điều trị tiếp: Hóa trị bổ trợ
Bàn luận:
Bệnh nhân được chẩn đoán ung thư vú (UTV) với một số yếu tố thuận lợi: giai đoạn sớm (IIA), u kích thước 2x1,8x1,5 cm, hạch viêm, thụ thể nội tiết dương tính.
Tuy nhiên bệnh nhân có yếu tố không thuận lợi là HER2 dương tính, khiến bệnh có nguy cơ tái phát tại chỗ và di căn cao, đặc biệt là xương và não. Bệnh nhân cao tuổi (75 tuổi), có bệnh lý tim mạch nhiều năm, có tiền sử đau vùng trước tim là yếu tố ảnh hưởng tới quyết định lựa chọn hóa chất điều trị bổ trợ do liên quan đến độc tính (nhất là độc tính trên tim mạch), khả năng dung nạp thuốc của bệnh nhân.
Về điều trị: Theo các hướng dẫn điều trị quốc tế như NCCN, ESMO, ASCO, bệnh nhân UTV có bộc lộ quá mức HER2 được chỉ định liệu pháp thuốc nhắm đích HER2 để cải thiện thời gian sống thêm, giảm tỷ lệ tái phát, di căn.1
Trastuzumab là một kháng thể đơn dòng đặc hiệu cho phần ngoại bào thụ thể HER2 đã được chứng minh hiệu quả giảm tái phát, tử vong trong nhiều thử nghiệm lâm sàng điều trị bổ trợ khi kết hợp với hóa trị.2
Các phác đồ hóa chất kết hợp trastuzumab đã chứng minh giảm nguy cơ tái phát, giảm nguy cơ tử vong nhưng làm tăng độc tính tim mạch. Trong các nghiên cứu lâm sàng bổ trợ, tỷ lệ suy tim sung huyết độ III/IV hoặc tử vong liên quan đến biến cố tim mạch trong phác đồ chứa trastuzumab trong khoảng từ 0% đến 4,1%.1-5 Tần suất xuất hiện suy tim liên quan đến tuổi và phân suất tống máu thất trái.
Các phác đồ hóa chất bổ trợ thường có anthracycline là nhóm thuốc có độc tính tim mạch tích lũy nên phối hợp hóa chất có anthracycline và trastuzumab càng làm tăng nguy cơ biến cố tim mạch.6,7
Phác đồ hóa trị không có anthracycline cũng đã được nghiên cứu nhằm giảm thiểu tác dụng ngoại ý trên tim mạch đã được chứng minh qua nghiên cứu BCIRG006 với 3.222 bệnh nhân có HER2 dương tính, hạch nách dương tính hoặc hạch nách âm tính nguy cơ cao. Trong nghiên cứu, bệnh nhân được phân ngẫu nhiên sử dụng 1 trong 3 phác đồ hóa trị: AC-T, AC-TH và TCH. Tại thời điểm theo dõi trung vị 65 tháng, nghiên cứu ghi nhận không có sự khác biệt có ý nghĩa thống kê dựa trên chỉ số nguy cơ cho DFS được quan sát trên 2 nhóm có sử dụng trastuzumab (81% ở nhóm TCH và 84% ở nhóm AC-TH). Lợi ích OS đã được ghi nhận ở cả 2 nhóm có sử dụng trastuzumab. Trong 2 nhóm có sử dụng trastuzumab, độc tính tim mạch thấp hơn đáng kể: Giảm phân suất tống máu thất trái (LVEF) >10% gặp ở 97 bệnh nhân trong nhóm điều trị TCH (9,4%) so với 194 bệnh nhân ở nhóm điều trị AC-TH (18,6%). Tỷ lệ suy tim sung huyết cũng gặp nhiều hơn ở nhóm điều trị AC-TH so với TCH (2% so với 0,4%).8,9
Vì vậy, phác đồ TCH có ưu thế trên nhóm bệnh nhân lớn tuổi, hay có bệnh lý tim mạch có nguy cơ suy tim.
Ở đây, bệnh nhân 75 tuổi có tiền sử bệnh lý tim mạch nhiều năm. Trong ca lâm sàng này, bệnh nhân có thụ thể nội tiết dương tính, HER2 dương tính nên được chỉ định hóa trị phác đồ TCH là thích hợp, không ảnh hưởng đến kết quả sống thêm mà giảm thiểu nguy cơ độc tính trên tim mạch so với việc dùng hóa trị có anthracycline.
Bệnh nhân được sử dụng phác đồ TCH liều:
- Docetaxel 75 mg/m2, mỗi 3 tuần x 6 chu kỳ
- Carboplatin AUC 6 mỗi 3 tuần x 6 chu kỳ
- Trastuzumab (liều tải 8 mg/kg, duy trì 6 mg/kg mỗi 3 tuần) x 1 năm (18 chu kỳ)
- Điều trị nội tiết với thuốc ức chế aromatase.
Bệnh nhân được làm xét nghiệm công thức máu, sinh hóa máu, chỉ điểm u CA 15-3 mỗi đợt trước truyền; làm xét nghiệm siêu âm tim, X-quang ngực, siêu âm bụng, hạch cổ, tuyến vú sau mỗi 3 chu kỳ trong 1 năm điều trị và 2 năm sau điều trị để theo tái phát, di căn và chức năng tim mạch.
Bệnh nhân dung nạp phác đồ điều trị khá tốt. Các triệu chứng mệt, rụng tóc, buồn nôn, tê bì tay chân thoáng qua không ảnh hưởng đến sinh hoạt. Không có tác dụng không mong muốn độ 3, độ 4 trên hệ tạo huyết, chỉ giảm bạch cầu (BC) độ 2 ở chu kỳ 4 và chu kỳ 5, không có sốt giảm BC. Bạch cầu hồi phục ngay sau sử dụng filgrastim, không phải giảm liều hóa chất, không phải kéo dài thời gian giữa 2 chu kỳ điều trị. Bệnh nhân không có cơn đau thắt ngực, siêu âm tim không có suy giảm phân số tống máu thất trái (EF%: 69% - 72%). Bệnh nhân đã theo được hết liệu trình điều trị 1 năm với trastuzumab với chất lượng cuộc sống không bị ảnh hưởng. Hiện nay, bệnh nhân đang ở năm thứ 4 sau điều trị. Tại lần tái khám định kỳ gần nhất, không có tái phát tại chỗ hay di căn xa được phát hiện.
Kết luận:
Phác đồ TCH là phác đồ hóa trị bổ trợ phù hợp để lựa chọn cho bệnh nhân ung thư vú có HER2 dương tính, đặc biệt trên nhóm bệnh nhân cao tuổi, có bệnh lý tim mạch đi kèm với hiệu quả cải thiện sống thêm và giảm thiểu tác dụng phụ.
- Piccart-Gebhart M, Procter M, Leyland-Jones B, et al. Trastuzumab after adjuvant chemotherapy in HER2-positive breast cancer. N Engl J Med 2005;353:1659-1672;
- Perez EA, Suman VJ, Davidson NE, et al. Cardiac safety analysis of doxorubicin and cyclophosphamide followed by paclitaxel with or without trastuzumab in the North Central Cancer Treatment Group N9831 adjuvant breast cancer trial. J Clin Oncol 2008;26:1231-1238;
- Joensuu H, KellokumpuLehtinen P, Bono P, et al. Adjuvant docetaxel or vinorelbine with or without trastuzumab for breast cancer. N Engl J Med 2006;354:809-820;
- Romond E, Suman V, Jeong J-H, et al. Trastuzumab plus adjuvant chemotherapy for HER2-positive breast cancer: Final planned joint analysis of overall survival (OS) from NSABP B-31 and NCCTG N9831. Cancer Research 2012;72:S5-5;
- Perez EA, Romond EH, Suman VJ, et al. Updated results of the combined analysis of NCCTG N9831 and NSABP B-31 adjuvant chemotherapy with/without trastuzumab in patients with HER2-positive breast cancer [abstract];
- Tan-Chiu E, Yothers G, Romond E, et al. Assessment of cardiac dysfunction in a randomized trial comparing doxorubicin and cyclophosphamide followed by paclitaxel, with or without trastuzumab as adjuvant therapy in node-positive, human epidermal growth factor receptor 2-overexpressing breast cancer: NSABP B-31. J Clin Oncol 2005;23:7811- 7819;
- Geyer CE, Jr., Bryant JL, Romond EH, et al. Update of cardiac dysfunction on NSABP B-31, a randomized trial of sequential doxorubicin/cyclophosphamide (AC)->paclitaxel (T) vs. AC->T with trastuzumab (H) [abstract]. J Clin Oncol 2006;24(Suppl 18):Abstract 581;
- Telli ML, Hunt SA, Carlson RW, Guardino AE. Trastuzumab-related cardiotoxicity: calling into question the concept of reversibility. J Clin Oncol 2007;25:3525-3533;
- Slamon D, Eiermann W, Robert N, et al. Adjuvant trastuzumab in HER2-positive breast cancer. N Engl J Med 2011;365:1273-1283.


