Luftvejsremodellering ved astma: Hvorfor IL‑4 og IL‑13 spiller en central rolle1,9
Luftvejsremodellering driver et progressivt og potentielt irreversibelt fald i lungefunktion hos patienter med astma.2 En forståelse af den centrale rolle, som IL‑4 og IL‑13 spiller i denne proces, er afgørende for at kunne målrette den mest effektive behandling.1,10
Lyt til Prof. Alberto Papi som fortæller om luftvejsremodellering
Hvad er luftvejsremodellering og airway hyperresponsiveness (AHR)?1,3-5
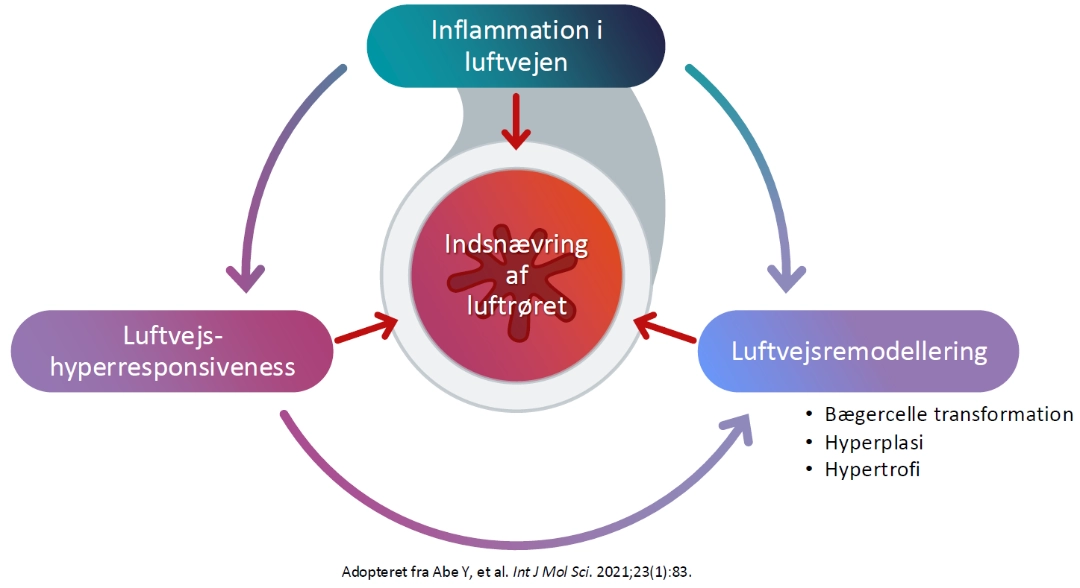
Astma involverer kronisk inflammation i luftvejene, strukturelle ændringer i luftvejene og hypertrofi af glat muskulatur.3,4 Disse processer - luftvejsremodellering og AHR - er nøglemekanismer bag det gradvise fald i lungefunktionsniveau.1,5
Type 2-inflammation, hyperresponsiveness og remodellering er med til at luftvejene indsnævres6 |
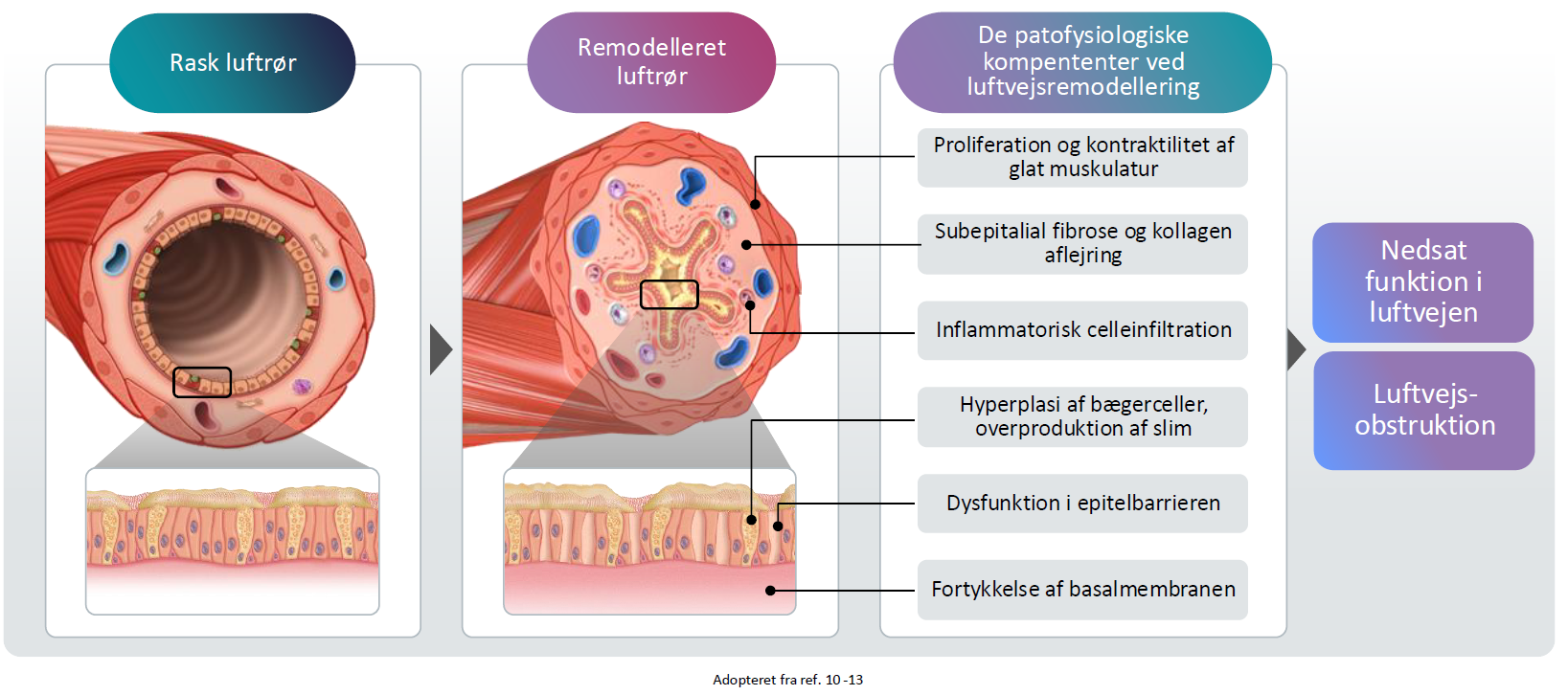
Luftvejsremodeling refererer til de progressive strukturelle forandringer i luftvejene, der opstår som følge af kronisk inflammation. Disse omfatter:
- Fortykkelse af den retikulære basalmembran – laget under epitelet bliver unormalt tykt
- Subepitelial fibrose – udvikling af arvæv under epitelet
- Hypertrofi af luftvejens glatte muskulatur (ASM) – muskulaturen øges i størrelse og medfører forsnævring af lumen
- Gobletcelle‑hyperplasi – øget antal mucinproducerende celler medfører overproduktion af mucus4
Remodellering ved astma omfatter strukturelle ændringer i luftvejene10-13
Airway hyperresponsiveness er luftvejens overdrevne tendens til at kontrahere som reaktion på stimuli. AHR opstår som resultat af øget kontraktilitet i glat muskulatur, vedvarende luftvejsinflammation og strukturelle ændringer forbundet med remodeling.3,5
Klinisk fører AHR til:
- accelereret fald i lungefunktion over tid
- tiltagende piben og vedvarende symptomer
- hyppigere og mere udtalte symptomer5
AHR indebærer en overdreven kontraktion af luftvejenes glatte muskulatur, som respons på stimuli, der ikke påvirker raske personer.
Vigtig klinisk indsigt |
AHR er forbundet med øget risiko for nedsat lungefunktion, vedvarende symptomer som hvæsen og forekomst af fremtidige eksacerbationer. Behandlingsstrategier, der normaliserer AHR, kan derfor reducere risikoen for eksacerbationer og forhindre yderligere inflammation og remodellering.5 |
Type 2-inflammation og dens rolle10
Hos langt størstedelen af patienter med astma er type 2‑inflammation den dominerende patofysiologiske mekanisme.10 Den drives primært af IL‑4, IL‑13 og IL‑5 samt epiteliale alarminer som TSLP og IL‑33.10
Hvordan driver type 2‑cytokiner astmapatologi?1-2,10-11
Den samlede effekt af IL‑4 og IL‑13 omfatter ødem, mucus‑hypersekretion, AHR og progressiv remodellering, hvilket fører til reduceret lungefunktion.10
Vidste du det? |
Eosinofile celler er IKKE de primære aktører for luftvejsremodellering. IL-4 og IL-13 er de cytokiner, der primært er ansvarlige for de strukturelle ændringer i luftvejene, der fører til nedsat lungefunktion. Det er afgørende at adressere disse cytokiner for at stoppe lungeskader.1,2 |
Hvilken rolle spiller hver type 2-cytokin i luftvejsremodelleringsprocessen?
IL-4 |
IL-13 |
IL-5 |
| Differentiering af T-celler og B-celler | ||
|
|
Differentiering af eosinofile celler i knoglemarven | |
| Migration og ekstravasation af eosinofile celler ind i lungernes luftveje | ||
| IgE-produktion og klasseskift;
degranulering af mastceller og basofile celler |
||
| Modning af gobletceller;
slimsekretion |
||
| Differentiering af bronkiale epitelceller | ||
| Øget kontraktilitet af glatte muskelceller i luftvejene og bronkial hyperresponsivitet | ||
BEMÆRK: Det thymiske stromale lymfopoletin (TSLP), et epital-afledt cytokin, bidrager til luftvejsombygning i lungerne ved at fremme forskellige processer og påvirke dendriske cellefunktion.
IL‑4 og IL‑13 som centrale terapeutiske mål1,8,9
Selvom eosinofiltal og IL‑5 er vigtige markører og mekanismer, er IL‑4 og IL‑13 de primære aktører af de strukturelle ændringer, der karakteriserer remodellering.2 Behandling, der blokerer IL‑4 og IL‑13 adresserer både inflammation og remodellering, reducerer luftvejs‑eosinofili, mindsker type 2‑associeret inflammation og påvirker sygdomsprogression mere grundlæggende end eosinofil‑reduktion alene.2 Dette gør IL‑4/IL‑13‑målrettet behandling til en central strategi for at modvirke fald i lungefunktion og bremse sygdomsprogression.2
Undersøgelser understøtter IL-4 og IL-13 påvirkning af luftvejsinflammation, AHR og luftvejsremodellering som vigtige terapeutiske mål for behandlingen.1,8,9
Sammenligning af terapeutiske mål
Mål |
Mekanisme |
Indvirkning på luftvejsremodellering |
| IL-4 & IL-131,2,9 | Fremmer luftvejsinflammation, eosinofilmigration og adhæsion, slimhypersekretion og AHR. | Direkte adressering af den grundlæggende årsag til remodellering og nedsat lungefunktion. |
| IL-51,2 | Medierer eosinofildifferentiering i knoglemarv og aktivering i luftvejene. | Sekundær rolle - påvirker remodelleringen gennem eosinofilmedierede inflammatoriske processer. |
Blokering af IL-4 og IL-13 kan også undertrykke eosinofil inflammation og indirekte reducere eosinofil i luftvejsvævet.1
Nøglebudskab |
Blokering af IL-4 og IL-13 kan reducere eosinofili i luftvejsvævet, mindske immuninfiltrater forbundet med type 2-inflammation og forlænge terapeutiske fordele ud over alene reduktion af eosinofiltallet.1,2 |
Kliniske implikationer: Betydningen af tidlig intervention7
Luftvejsremodellering er en progressiv proces. Tidlig identifikation af type 2‑inflammation kan hjælpe klinikeren med at identificere patienter med høj risiko for remodellering og vælge en behandling, der adresserer de underliggende mekanismer.7
Vigtige type 2‑biomarkører:7
- Blod‑eosinofile celler - forhøjet værdier indikerer eosinofil luftvejsinflammation
- Fraktioneret nitrooxygen i udåndingsluften (FeNO) - markør for IL‑13‑medieret inflammation
- Serum‑IgE - forhøjet ved allergisk/type 2-astma
Proaktiv diagnostik og tidlig målrettet intervention kan forbedre sygdomsforløbet og reducere risiko for irreversibelt lungefunktionsfald.7
Klinisk handling |
Identificer dine patienter med risiko for luftvejsremodellering ved tidlig vurdering af type 2-biomarkører. Proaktiv fænotypebestemmelse og målrettet behandling kan forbedre sygdomsprogressionen.7 |
Lyt til professor Alberto Papi om vigtigheden af tidlig intervention
-
Nakagome K, Nagata M. The Possible Roles of IL-4/IL-13 in the Development of Eosinophil-Predominant Severe Asthma. Biomolecules. 2024;14(5):546. Published 2024 May 2. doi:10.3390/biom14050546
-
Scott G, Asrat S, Allinne J, et al. IL-4 and IL-13, not eosinophils, drive type 2 airway inflammation, remodeling and lung function decline. Cytokine. 2023;162:156091. doi:10.1016/j.cyto.2022.156091
-
Bradding P, Porsbjerg C, Côté A, Dahlén SE, Hallstrand TS, Brightling CE. Airway hyperresponsiveness in asthma: The role of the epithelium. J Allergy Clin Immunol. 2024;153(5):1181-1193. doi:10.1016/j.jaci.2024.02.011
-
Hough KP, Curtiss ML, Blain TJ, et al. Airway Remodeling in Asthma. Front Med (Lausanne). 2020;7:191. Published 2020 May 21. doi:10.3389/fmed.2020.00191
-
Chapman DG, Irvin CG. Mechanisms of airway hyper-responsiveness in asthma: the past, present and yet to come. Clin Exp Allergy. 2015;45(4):706-719. doi:10.1111/cea.12506
-
Abe Y, Suga Y, Fukushima K, et al. Advances and Challenges of Antibody Therapeutics for Severe Bronchial Asthma. Int J Mol Sci. 2021;23(1):83. Published 2021 Dec 22. doi:10.3390/ijms23010083
-
Zhang J, Dong L. Status and prospects: personalized treatment and biomarker for airway remodeling in asthma. J Thorac Dis. 2020;12(10):6090-6101. doi:10.21037/jtd-20-1024
-
León B, Ballesteros-Tato A. Modulating Th2 Cell Immunity for the Treatment of Asthma. Front Immunol. 2021;12:637948. Published 2021 Feb 10. doi:10.3389/fimmu.2021.637948
-
Pelaia C, Heffler E, Crimi C, et al. Interleukins 4 and 13 in Asthma: Key Pathophysiologic Cytokines and Druggable Molecular Targets. Front Pharmacol. 2022;13:851940. Published 2022 Mar 8. doi:10.3389/fphar.2022.851940
-
Gandhi NA, et al. Nat Rev Drug Discov. 2016;15(1):35-50.
-
Israel E, Reddel HK. N Engl J Med. 2017;377(3):965-976.
-
Mauad T, et al. J Allergy Clin Immunol. 2007;120(5):997-1009.
-
Robinson D, et al. Clin Exp Allergy. 2017;47(2):161-175.