De kracht om de chaos van RSV te verminderen1-4

Alle zuigelingen lopen risico op respiratoir syncytieel virus (RSV) en aandoeningen van de lagere luchtwegen (LRTD)*5-11, maar we kunnen niet voorspellen wie getroffen zal worden.12
RSV aandoening van de onderste luchtwegen (LRTD) is een belangrijke oorzaak van ziekenhuisopname bij zuigelingen, ongeacht de gezondheidstoestand, de zwangerschapsduur bij de geboorte of de geboortemaand.**, 5-11,13-16
Beyfortus® is terugbetaald voor baby’s ter preventie van RSV¤
Raadpleeg de aanvraagformulieren voor de baby’s;
Karakteristieken van baby's met ziekenhuisopnames voor RSV
|
|
|
Beyfortus®: de kracht om de chaos van RSV te verminderen
Beyfortus® vermindert het risico op medisch begeleide RSV-infectie van de onderste luchtwegen (LRTD), inclusief ziekenhuisopname, bij zuigelingen.1
Beyfortus® is de eerste en enige RSV-immunisatie die is ontworpen voor alle zuigelingen, ter bescherming tegen RSV LRTD.1
Beyfortus® is ontworpen voor bescherming van zuigelingen tegen aandoeningen van de lagere luchtwegen (LRTD) veroorzaakt door respiratoir syncitieel virus (RSV) gedurende het eerste RSV-seizoen, via één enkele toediening van antilichamen.1
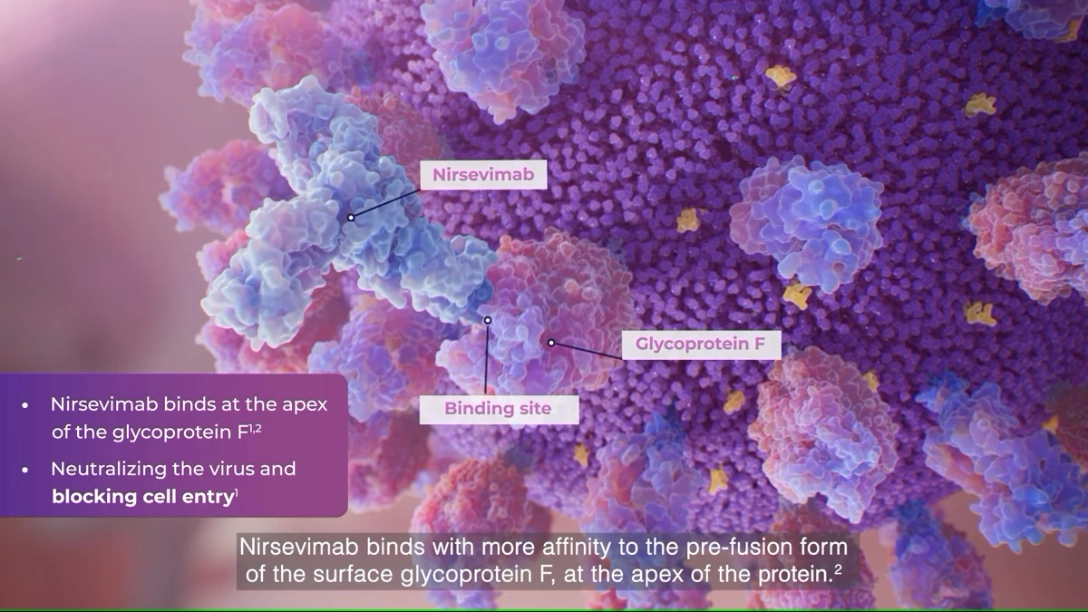
Beyfortus® is een direct, langwerkend antilichaam1
|
|
|
|
Bekijk de video om meer te weten te komen over de werking van Beyfortus®
Beyfortus® werd ontwikkeld voor een brede populatie van zuigelingen1-4,18
Dit omvatte voldragen of premature baby's, geboren tijdens of voor het RSV-seizoen, gezonde baby's of met aangeboren hartaandoeningen en chronische longaandoeningen door prematuriteit.1-4,18
|
|
|
|
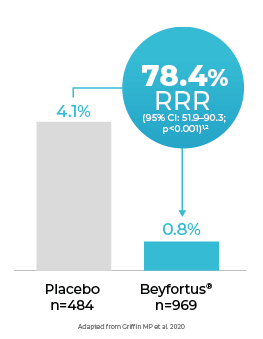
Beyfortus® vermindert het risico op ziekenhuisopnames voor RSV LRTD
Hieronder vind je een overzicht van de relatieve risicoreductie (RRR) van ziekenhuisopnames voor RSV LRTD tot 150 dagen na toediening in Fase 2b en MELODY studies, tijdens het RSV seizoen voor HARMONIE studie.
Veiligheid
De veiligheid is onderzocht bij een brede populatie, waaronder gezonde premature, mature baby's en baby's met een hoger risico op RSV-infecties van de lagere luchtwegen (LRTDs). De soorten en frequentie van bijwerkingen (AE's) met Beyfortus® waren vergelijkbaar met placebo in de fase 2b- en fase 3-studies.2-4,19
De meest voorkomende bijwerking was rash (0,7%) die binnen 14 dagen na toediening optrad. Het merendeel van deze bijwerking was licht tot matig van intensiteit. Aanvullend werden pyrexie en injectieplaatsreacties binnen 7 dagen na toediening gemeld met een prevalentie van respectievelijk 0,5% en 0,3%. Injectieplaatsreacties waren niet ernstig.1
Bijwerkingen gemeld bij 2.966 voldragen - en premature baby's (zwangerschapsduur [GA] ≥29 weken) die Beyfortus® kregen in twee placebogecontroleerde klinische onderzoeken1
| Systeem-Orgaanklasse | Bijwerking | Frequentie |
| Huid- en onderhuidaandoeningen | Rash | Soms |
| Algemene aandoeningen en toedieningsplaatsstoornissen | Reactie op de injectieplaats | Soms |
| Pyrexie | Soms |
Op basis van Beyfortus® samenvatting van de productkenmerken BE (11/2023). De frequentie van soms is tussen ≥ 1/1.000 tot < 1/100.
In de studie van zuigelingen met een hoger risico op ernstige RSV-ziekte was het veiligheidsprofiel van Beyfortus® vergelijkbaar met dat van palivizumab en consistent met dat van de studies bij gezonde, voldragen en te vroeg geboren baby's (≥ 29 weken GA).‡,1,2
Raadpleeg SPK voor waarschuwingen en voorzorgsmaatregelen bij gebruik.‡
De toediening moet samenvallen met het eerste RSV-seizoen van een zuigeling1 - de periode met het grootste risico op LRTD.20
Hoe gebruikt u Beyfortus® ?
Beyfortus® maakt een flexibele implementatie mogelijk.
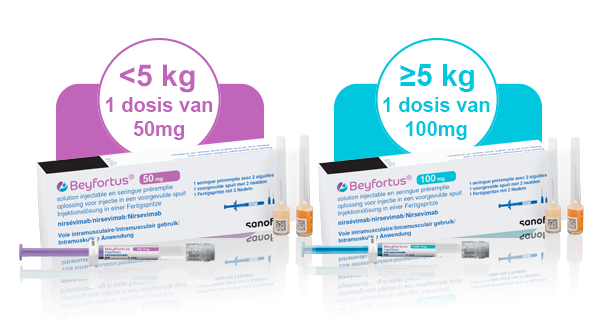
Beyfortus® is terugbetaald voor alle pasgeborenen en zuigelingen jonger dan 13 maanden voor het eerste RSV-seizoen in de volgende dosering:
Eenmalige toediening
Gebaseerd op het gewicht van de zuigeling op het moment dat Beyfortus® wordt toegediend.****,1
Beyfortus® wordt intramusculair geinjecteerd, bij voorkeur in het anterolaterale aspect van de dij.*****,1
Voor kinderen die kwetsbaar blijven voor ernstige RSV-ziekte in hun tweede RSV-seizoen 200 mg toegediend als 2 injecties van 100 mg op afzonderlijke plaatsen.
Beyfortus® moet voor het RSV-seizoen worden gegeven. Het virus komt meestal vaker voor gedurende de winter (staat bekend als het RSV-seizoen). Als uw kind tijdens de winter geboren wordt, moet dit middel na de geboorte worden gegeven.1

Praktische overwegingen
* Percentage kinderen gezond en/of voldragen geboren onder kinderen opgenomen in het ziekenhuis vanwege RSV in verschillende retrospectieve analyses: Frankrijk (2010-2018; bij kinderen <5 jaar): 87% gezond en 90% voldragen;5 Spanje (2004-2012; bij zuigelingen): 98% gezond en voldragen;6 Japan (januari 2017-december 2018; bij kinderen ≤2 jaar): 90% gezond en voldragen;7 Duitsland (2015-2018; bij zuigelingen): 90% gezond en 83% voldragen;8 China (2007-2015, bij kinderen 28 dagen-13 jaar): 88% gezond en voldragen termijn (mediane leeftijd 1,4 jaar):9 VK (Schotland 2000-2011; bij kinderen ≤2 jaar): 93% gezond en 82% voldragen;10 VS (population-based surveillance 2014-2015; bij zuigelingen ≤11 maanden): 72% gezond en voldragen.11
** Uit retrospectieve analyses uitgevoerd in Frankrijk (45.225 RSV-geassocieerde ziekenhuisopnames per seizoen tussen 2010 en 2018)5 en de VS (243.834 RSV bronchiolitis, 38.064 RSV pneumonie en 15.786 andere RSV-ontslagen bij zuigelingen <1 jaar tussen 1997 en 1999).13
*** Gebaseerd op klinische en farmacokinetische gegevens.1
**** De aanbevolen dosis is een eenmalige dosis van 50 mg intramusculair toegediend voor zuigelingen met een lichaamsgewicht <5 kg en een eenmalige dosis van 100 mg intramusculair toegediend voor zuigelingen met een lichaamsgewicht ≥5 kg.1 Raadpleeg de samenvatting van de productkenmerken voor volledige informatie over dosering en toedieningsinformatie.
***** De bilspier mag niet routinematig als injectieplaats worden gebruikt vanwege het risico op beschadiging van de nervus ischiadicus.1
+ Gebaseerd op een Engels onderzoek waar 51% (n=10.328/20.359) van de ziekenhuisopnames als gevolg van RSV voorkwamen bij zuigelingen die geboren waren voor het seizoen (april tot oktober);15 een Spaans onderzoek waar 54% (n=340/631) van de met RSV opgenomen zuigelingen geboren waren voor het seizoen (april tot oktober);14 en een Frans onderzoek waar 47% (n=85.292/181.758) van de met RSV opgenomen zuigelingen geboren waren voor het seizoen (april tot oktober).5
‡ De veiligheid werd geëvalueerd in MEDLEY bij 918 zuigelingen met een verhoogd risico op ernstige RSV-ziekte, waaronder 196 extreem premature zuigelingen (GA <29 weken) en 306 zuigelingen met chronische longziekte van prematuriteit, of "hemodynamisch significante aangeboren hartziekte die hun eerste RSV-seizoen ingingen, die nirsevimab (614) of palivizumab (304) kregen.1
¤ Raadpleeg de website van het RIZIV voor meer informatie over de terugbetalingsvoorwaarden van Beyfortus®: https://webappsa.riziv-inami.fgov.be/ssp/ProductSearch
Referenties
-
Samenvatting van de productkenmerken Beyfortus® - 04/2024
-
Griffin MP et al. N Engl J Med 2020; 383(5): 415-425
-
Domachowske J et al. N Engl J Med 2022; 386(9): 892-894
-
Hammitt LL et al. N Engl J Med 2022; 386(9): 837-846
-
Demont C et al. BMC Infect Dis 2021; 21(1): 730.
-
Sanchez-Luna M et al. Curr Med Res Opin 2016; 32(4): 693-698.
-
Kobayashi Y et al. Ped Intl 2021; 64(1): e 14957.
-
Yu Jet al. Emerg Infect Dis 2019; 25(6): 1127-1135.
-
Hartmann K et al. J Infect Dis 2022; 226(3): 386-395.
-
Arriola C et al. J Pediatric Infect Dis Soc 2020; 9(5): 587-595.
-
Thwaites R et al. Eur J Pediatr 2020; 179(5): 791-799.
-
Bianchini S et al. Microorganisms 2020; 8(12): 2048
-
Leader S and Kohlhase K. Pediatr Infect Dis J 2002; 21(7): 629-632.
-
Mira-Iglesias A et al. Influenza Other Respir Viruses 2022; 16(2): 328-339.
-
Reeves RM et al. J Infect 2019; 78(6): 468-475.
-
Gantenburg JR et al. J Infect Dis 2022; 226(Suppl 2): S164-S174.
-
Heinonen S et al. Immunol Allergy Clin North Am 2019; 39(3): 361-376.
-
Drysdale SB et al. N Eng J Med 2023; 389: 2425-2435 & Protocol.
-
Muller WJ et al. N Engl J Med 2023; 388(16): 1533-1534.
-
Esposito S et al. Front Immunol 2022; 13: 880368.