Vestige studiet
Mucus plugging og astma. Få mere indsigt i dette område her.

VESTIGE STUDIET VAR DET STØRSTE STUDIE SOM ANVENDER NY FUNKTIONEL RESPIRATORISK BILLEDTEKNOLOGI (FRI) TIL ASTMAPATIENTER I BIOLOGISK BEHANDLING2
VESTIGE var et fase 4, multinationalt, randomiseret, dobbeltblindet, placebokontrolleret billeddiagnostisk studie, der vurderede effekten af dupilumab på luftvejsinflammation og strukturelle ændringer i luftvejene hos patienter med ukontrolleret moderat til svær astma.1*
Video om studiedesignet
Studieresultater præsenteret af Prof. Castro
Primære endepunkter1

Type 2 luftvejsinflammation
Andel af patienter, der opnåede FeNO <25 ppb ved uge 24

Luftvejsvolumen
Procentvis ændring fra baseline til uge 24 i luftvejsvolumen (siVaw) ved total lungekapacitet (TLC)
Vigtigste sekundære endepunkter1

Mucus-score
Ændring i global slimscore fra baseline ved uge 24 bestemt ved højopløsnings computertomografi (HRCT)

Luftvejsmodstand
Procentvis ændring fra baseline til uge 24 i luftvejsmodstand (siRaw) ved total lungekapacitet (TLC)

Reduceret volumen og øget modstand i luftvejene er forbundet med remodellering af luftvejene3,4
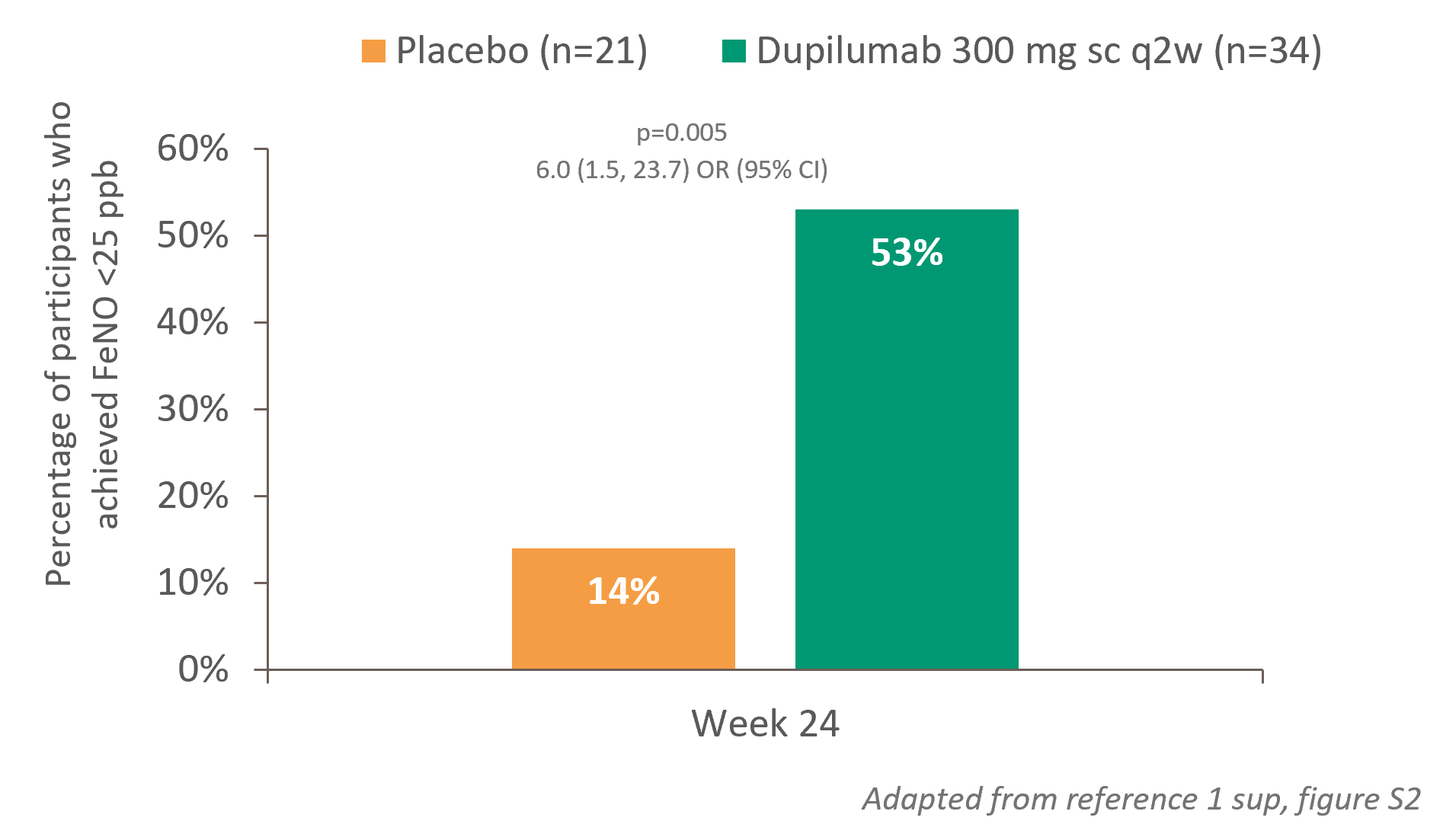
Normaliseret FeNO, en biomarkør for type 2-inflammation1
53%
AF PATIENTER PÅ DUPIXENT OPNÅEDE FENO <25 ppb VED UGE 241,a,b
6x højere sandsynlighed for at opnå lavere FeNO hos patienter, der fik DUPIXENT sammenlignet med dem, der fik placebo1,a,b
Dupixent normaliserede FeNO vs placebo ved uge 241,a,b

Patienter som har høj FeNO:
- kan have op til 2,7 x højere risiko for hurtigt fald i FEV15,6
- har 50% større risiko for at få hyppigere eksacerbationer5,6
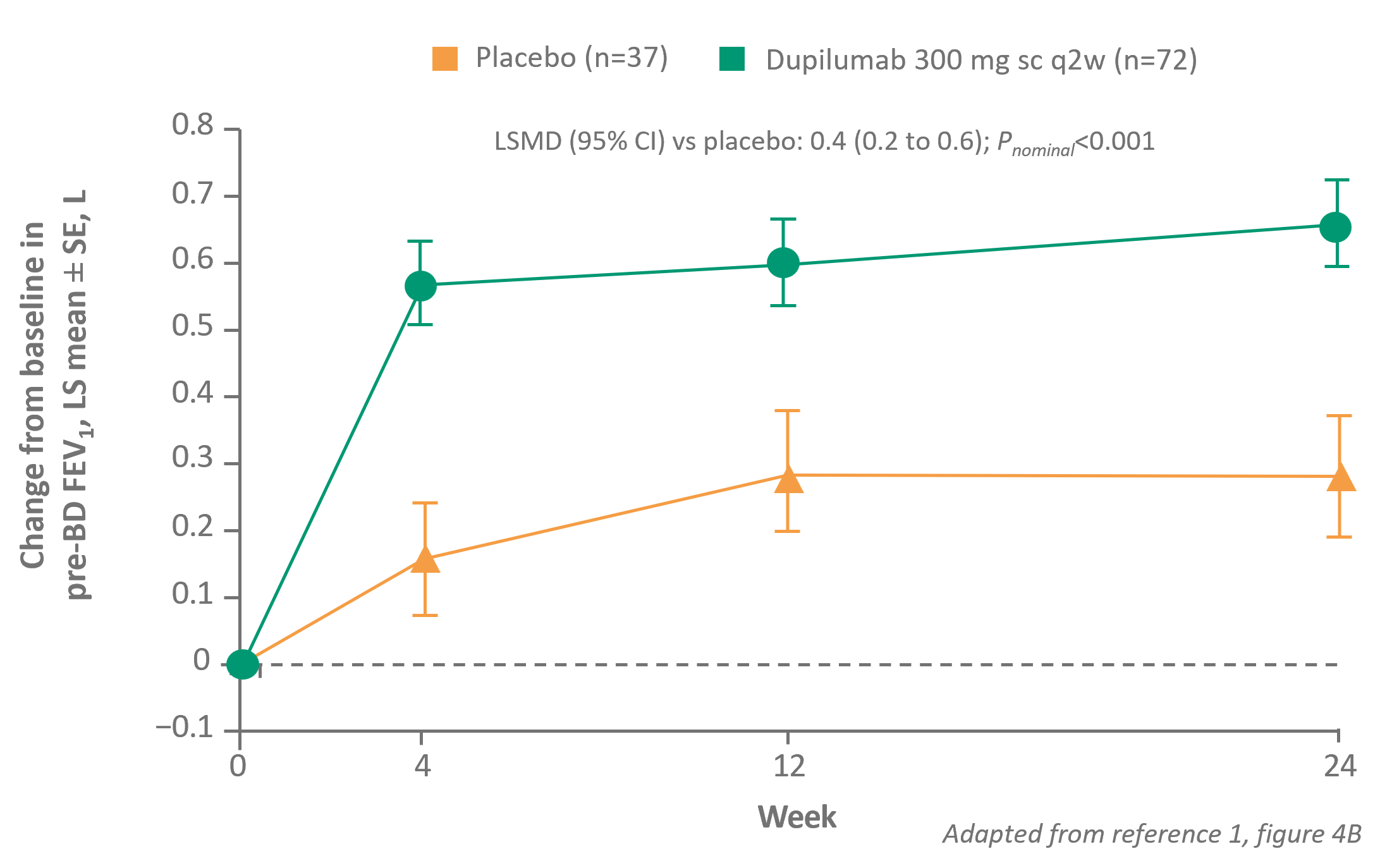
Forbedret lungefunktion1
Dupixent forbedrede lungefunktionen vs placebo fra uge 41
Forbedring af lungefunktion var forbundet med øget luftvejsvolumen1
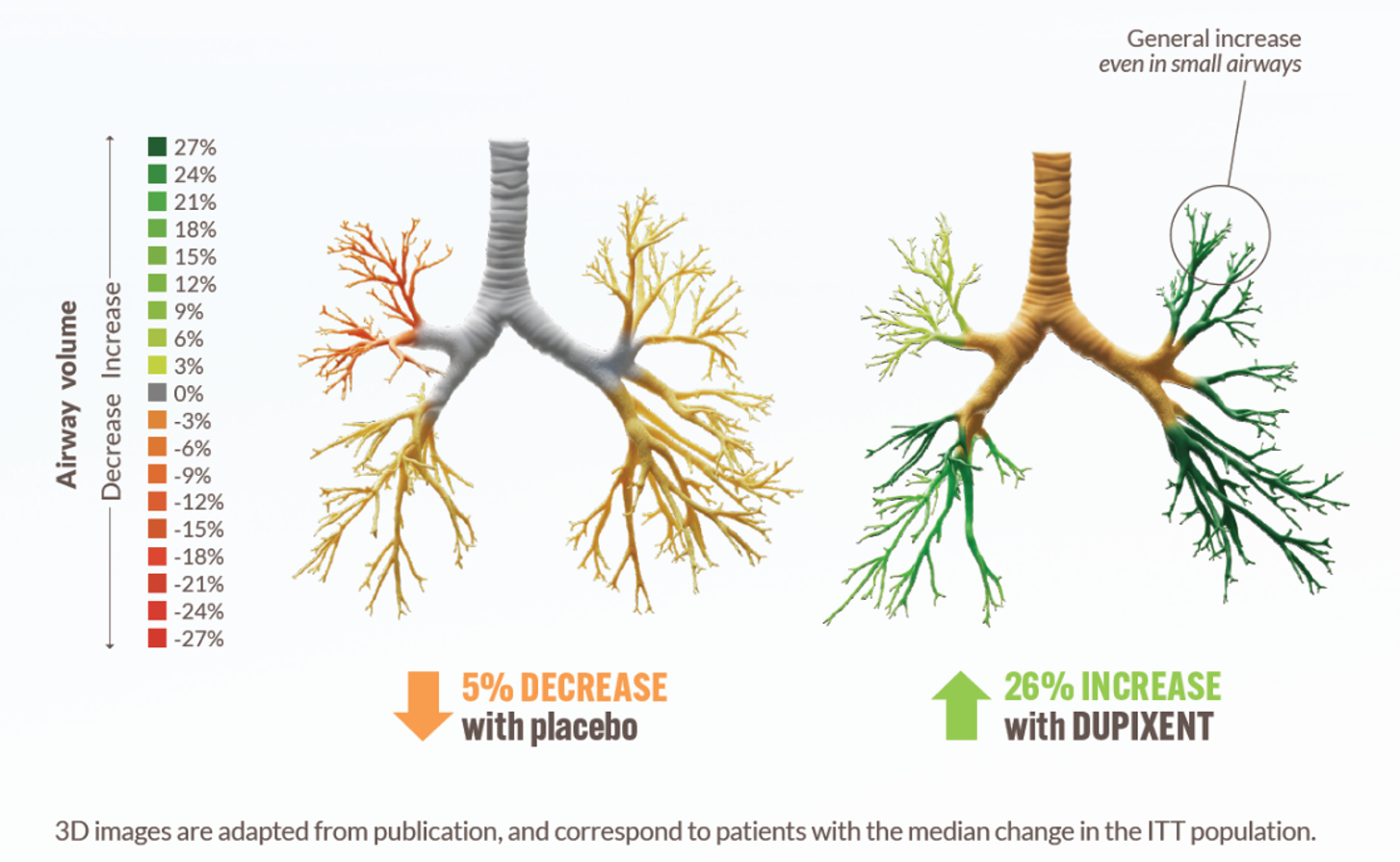
26%
ØGET LUFTVEJSVOLUME HOS PATIENTER SOM FIK DUPIXENT VED UGE 241,c,d
p=ns
Dupixent forbedrede nummerisk luftvejsvolumen vs placebo ved uge 241,c,d
Ændringer fra baseline til uge 24 i siVaw ved TLC
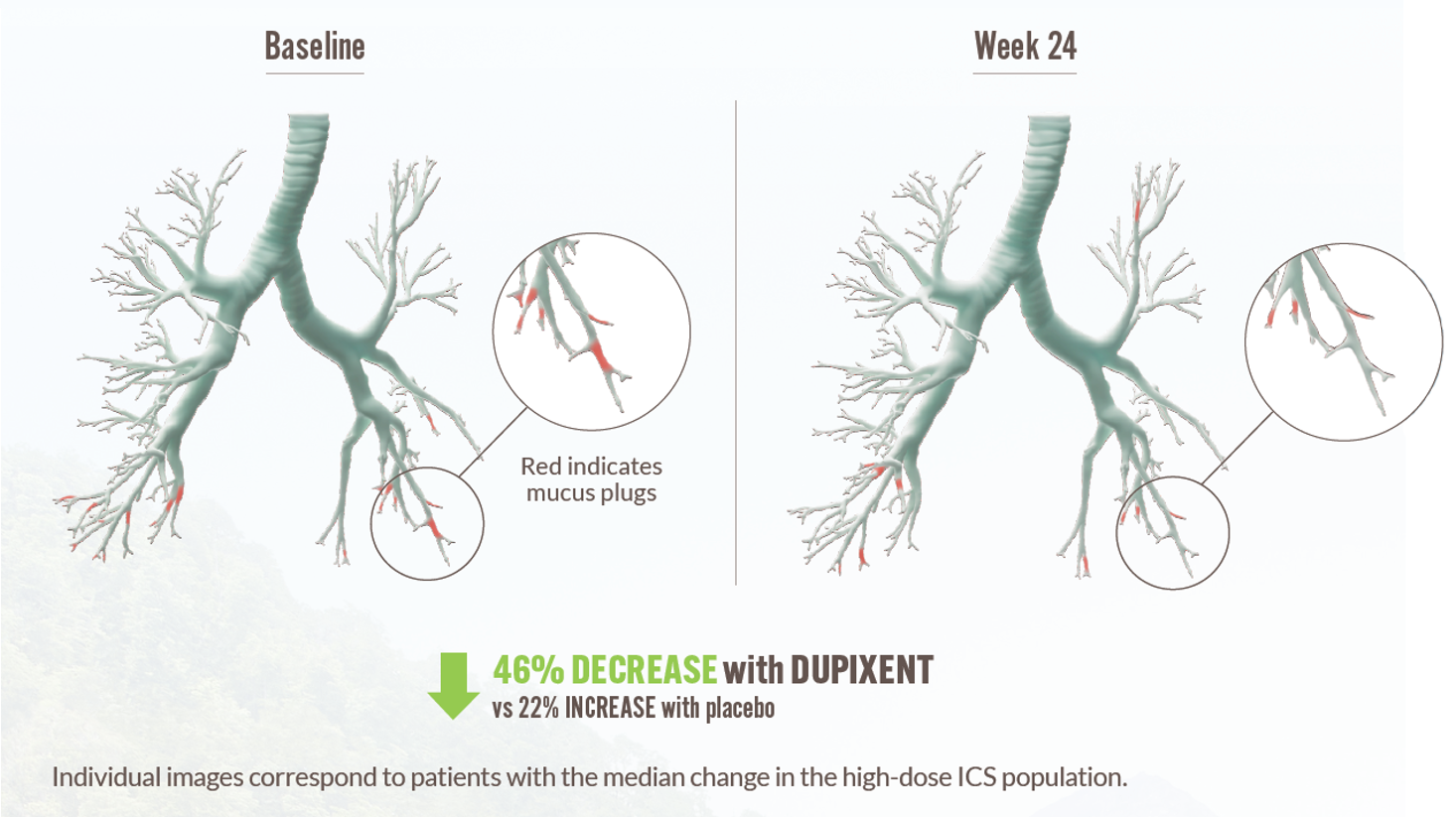
Forbedring af lungefunktion var tydeligt forbundet med reduktion af mucus plugging1,7
46%
AF PATIENTER SOM FIK DUPIXENT OPLEVEDE REDUKTION I MUCUS-SCORE VED UGE 241,e,f
-5,3 points ændring i mucus-score fra baseline til uge 24 grundet antiinflammatorisk effekt via direkte hæmning af IL-131,e,f
Dupixent reducerede signifikant mucus-scoren sammenlignet med placebo ved uge 241,e,f
Ændring fra baseline til uge 24 i mucus-score ved TLC
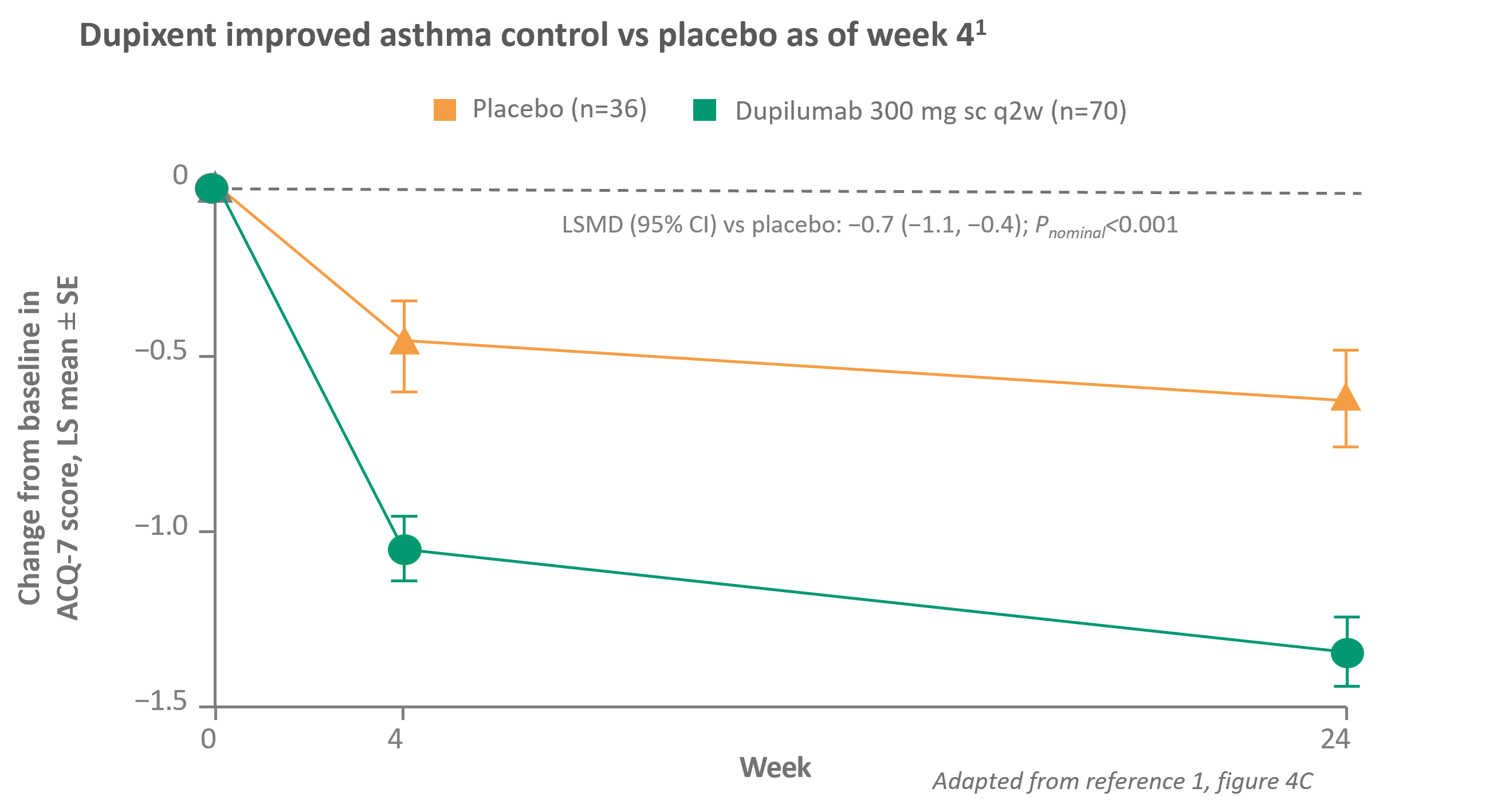
Forbedret astmakontrol1

DUPIXENT REDUCERER TYPE 2- INFLAMMATION OG FORBEDRER LUFTVEJSSTRUKTURER VED AT BLOKERE IL-4 OG IL-13 SIGNALERING8-11
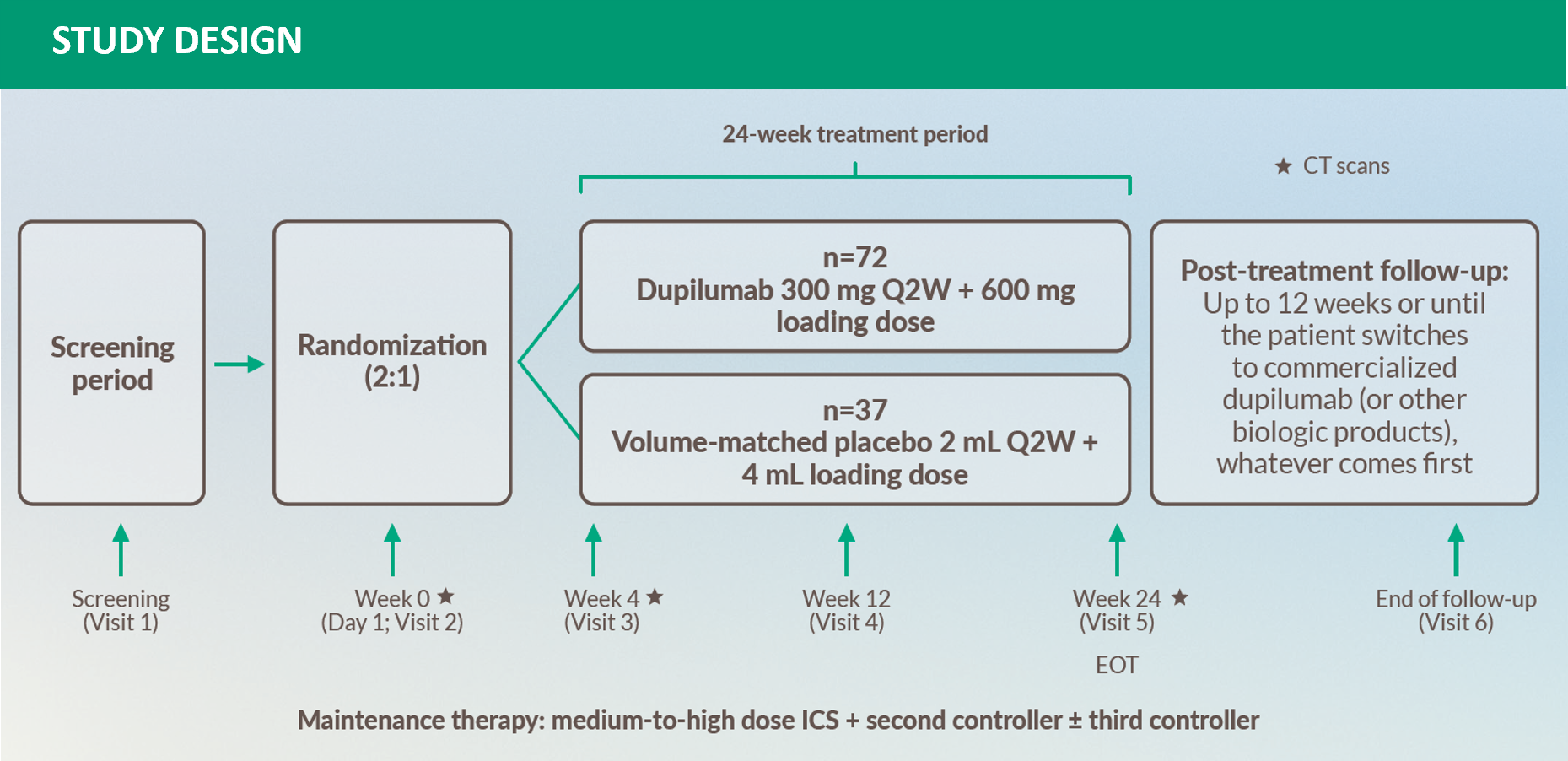
STUDIEPOPULATION
VESTIGE-studiepopulationen bestod af patienter i alderen 18 til 70 år med ukontrolleret moderat til svær astma (Astma Kontrol Spørgeskema [ACQ]-5 score ≥1.5), præ-BD FEV1 ≤80% af den forudsagte værdi, 1 eksacerbation det foregående år, blod-eosinofilantal ≥300 celler/μL og FeNO ≥25 ppb.1
HVAD ER FUNKTIONEL RESPIRATORISK IMAGINE(FRI)?
FRI er en ny computermodelingsteknik, der kombinerer højopløsnings CT-billeddannelse med computerfluiddynamik for at skabe patient-specifikke 3D-modeller af lungestruktur og funktion.
RATIONALE
- Kronisk luftvejsinflammation er til stede hos de fleste patienter med astma og er forbundet med øget slimproduktion, luftvejs hyperreaktivitet, glat muskelkontraktion og strukturel remodellering1
- Dupixent er det eneste biologiske lægemiddel, der direkte påvirker IL-4 og IL-13 signalering for at reducere type 2- inflammation med dokumenteret effekt på:
- Reduktion af eksacerbationer12
- Forbedring af lungefunktion12
- Reduktion eller eliminering af OCS, mens astmakontrollen opretholdes13
DUPIXENT ER DET ENESTE BIOLOGISKE LÆGEMIDDEL, DER DIREKTE PÅVIRKER IL-4 OG IL-13 SIGNALERING FOR AT REDUCERE TYPE 2 INFLAMMATION8,11,14
For mere information, klik her for at se Dupixent SmPC/pligttekst.
FeNO, fraktionen af ekshaleret nitrogenoxid — FeNO ≥25 ppb betragtes som unormalt; præ-BD FEV1, præbronchodilatorisk forceret ekspiratorisk volumen i 1 sekund; FRI, funktionel respiratorisk billeddannelse - en ny, ikke-invasiv teknologi, der bruger 2 forskellige billedteknologier til at skabe en detaljeret 3D-model af en patients lunge for at vurdere både luftvejsstruktur og lungefunktion; ICS, inhalerede kortikosteroider; ITT, intention-to-treat; LSMD, mindste kvadraters gennemsnitsforskel; Q2W, hver anden uge; siRaw, trimmet distal luftvejsmodstand korrigeret for lungevolumen; siVaw, specifikke regionale luftvejsvolumener korrigeret for lungevolumen; SOC, standardbehandling; TLC, total lungekapacitet.
* (ACQ-5≥1.5; præ-BD FEV1≤80% af forudsagt normalværdi, FeNO niveau ≥ 25 ppb, blod-eosinofiltal ≥300 celler/uL og ≥ 1 eksacerbation det foregående år)1
a I den højdosis ICS-population opnåede 53% af patienterne FeNO <25 ppb ved uge 24 med DUPIXENT 300 mg + SOC (n=34) vs 14% med placebo + SOC (n=21) (OR: 6,01; 95% CI: 1,53, 23,67, P=0,005)1
b I ITT-populationen opnåede 57% af patienterne FeNO <25 ppb med DUPIXENT 300 mg + SOC (n=72) vs 11% med placebo + SOC (n=37) (OR: 9,81; 95% CI: 3,13, 30,82, nominal P<0,001)1
c I den højdosis ICS-population var der en +26,1% ændring i luftvejsvolumen fra baseline ved uge 24 med DUPIXENT 300 mg + SOC (n=34) vs -4,8% med placebo + SOC (n=21) (LSM forskel, 31,0%; 95% CI: -12,7, 74,6). Numerisk større forbedring. P=NS.1
d I ITT-populationen var der en +20% ændring i luftvejsvolumen fra baseline ved uge 24 med DUPIXENT 300 mg + SOC (n=72) vs med placebo + SOC (n=37) (LSM forskel, 21,8%; 95% CI: -7,7, 51,3). Numerisk større forbedring. P=NS.1
e I den højdosis ICS-population var der en -3,8 points ændring i slimscore fra baseline ved uge 24 med DUPIXENT 300 mg + SOC (n=34) vs +1,5 points med placebo + SOC (n=21) (LSM forskel, -5,3; 95% CI: -7,7, 2,8, P<0,0001).1
f I ITT-populationen var der en -3,5 points ændring i slimscore fra baseline ved uge 24 med DUPIXENT 300 mg + SOC (n=63) vs +1,4 points med placebo + SOC (n=31) (LSM forskel, -4,9; 95% CI: -6,5, -3,3, P<0,001).1
-
Castro M, et al. Effect of dupilumab on exhaled nitric oxide, mucus plugs, and functional respiratory imaging in patients with type 2 asthma (VESTIGE): a randomised, double-blind, placebo-controlled, phase 4 trial; Published Online February 10, 2025; doi.org/10.1016/S2213-2600(24)00362-X.
-
De Prado Gomez L, et al. A randomized, double-blind, placebo-controlled study to evaluate the effect of dupilumab on airway remodeling in patients with uncontrolled, moderate-to-severe asthma: The VESTIGE Study. Chest. 2021;160(4):A1492-A1495.doi.org/10.1016/j.chest.2021.07.1367.
-
Berair R, et al. Associations in asthma between quantitative computed tomography and bronchial biopsy-derived airway remodelling. Eur Resp J. 2017;49(5):1601507. doi:10.1183/13993003.01507-2016
-
Chan R, et al. Impaired respiratory system resistance and reactance are associated with bronchial wall thickening in persistent asthma. J Allergy Clin Immunol Pract. 2023;11(5):1459-1462.e3. doi:10.1016/j.jaip.2022.12.040.
-
Matsunaga K, et al. Persistently high exhaled nitric oxide and loss of lung function in controlled asthma. Allergol Int. 2016;65(3):266-271. doi:10.1016/j.alit.2015.12.006
-
Yang F, et al. Factors associated with frequent exacerbations in the UK severe asthma registry. J Allergy Clin Immunol Pract. 2021;9(7):2691-2701.e1. doi:10.1016/j.jaip.2020.12.062.
-
Tang M, et al. Mucus plugs persist in asthma, and changes in mucus plugs associate with changes in airflow over time. Am J Respir Crit Care Med. 2022;205(9):1036- 1045. doi:10.1164/rccm.202110-2265OC.
-
DUPIXENT Summary of Product Characteristics.
-
Robinson D, et al. Revisiting type 2-high and type 2-low airway inflammation in asthma: current knowledge and therapeutic implications. Clin Exp Allergy. 2017;47(2):161-175. doi:10.1111/cea.12880.
-
Hammad H, et al. Dendritic cells and epithelial cells: linking innate and adaptive immunity in asthma. Nat Rev Immunol. 2008;8(3):193-204. doi:10.1038/nri2275.
-
Gandhi NA, et al. Targeting key proximal drivers of type 2 inflammation in disease. Nat Rev Drug Discov. 2016;15(1):35-50.doi:10.1038/nrd4624.
-
Pavord ID, et al. Dupilumab sustains efficacy in patients with moderate-to-severe type 2 asthma regardless of inhaled corticosteroids dose. Allergy. 2023;78(11):2921-2932. doi:10.1111/all.15792
-
Sher LD, et al. Dupilumab reduces oral corticosteroid use in patients with corticosteroid-dependent severe asthma: an analysis of the phase 3, open-label extension TRAVERSE trial. Chest. 2022;162(1):46-55. doi:10.1016/j.chest.2022.01.071.
-
Brusselle GG, et al. Biologic therapies for severe asthma. N Engl J Med. 2022;386(2):157-171. doi:10.1056/NEJMra2032506.
-
Scott G, et al. IL-4 and IL-13, not eosinophils, drive type 2 airway inflammation, remodeling and lung function decline. Cytokine. 2023;162:156091. doi:10.1016/j.cyto.2022.156091.
-
Bonser LR, et al. Epithelial tethering of MUC5AC-rich mucus impairs mucociliary transport in asthma. J Clin Invest. 2016;126(6):2367-2371. doi:10.1172/JCI84910.
-
Maspero J, et al. Type 2 inflammation in asthma and other airway diseases. ERJ Open Res. 2022;8(3):00576-2021. doi:10.1183/23120541.00576-2021